来源:莫罗单抗丨作者:Craig,Klaith
循环肿瘤细胞检测(CTC)是液体活检领域比较成熟的技术。本篇介绍CTC的概念、特性以及应用的案例。
早在1869年,澳大利亚医生ThomasAshworth观察一例转移性癌症患者的外周血,发现了循环肿瘤细胞。此后的100多年里,各国科学家不断努力,逐渐解开了循环肿瘤细胞的秘密,验证了其在肿瘤检测中的作用。
随着实体肿瘤的生长,周围微环境发生特定变化,部分肿瘤细胞会出现异常的上皮间质转化现象(英文缩写EMT,指上皮细胞到间质细胞的转化,使转化细胞具备转移和入侵的能力,例如形成干细胞特征、减少凋亡与衰老、促进免疫抑制等。间质细胞不仅在人体发育过程中起着关键的作用,还参与组织愈合、器官纤维化和癌症发生等过程)。这些从原发肿瘤上脱落,经由血液系统或淋巴系统去往身体各处的细胞被称为循环肿瘤细胞(CirculatingTumorCells,简称CTC)。CTC到达适宜的目的地后再次发生间质上皮转化(英文缩写MET),重新获得上皮细胞的增殖特性,形成转移灶,开始恶性繁殖。CTC从“逃跑”到“另起炉灶”,至少经历逃避身体免疫系统监视、克服肿瘤细胞自身代谢障碍、再次从血管或淋巴管中溢出、到达特定器官定植等过程。
图1 CTC的转移过程
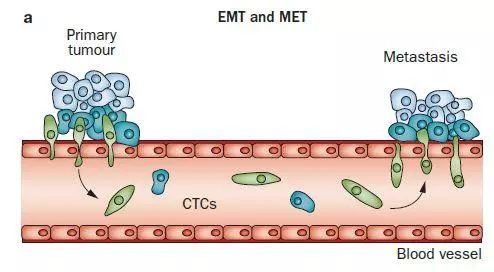
因此,当血液中检测到CTC时,说明肿瘤细胞已从原发部位脱落并进入了血液(但外周血检测到肿瘤细胞并不能说明肿瘤已发生了转移)。
1.稀有性
并不是所有进入血液的CTC都具有转移潜能,它们中的大多数进入血管后凋亡并被清除,只有不到0.1%的CTC最终转移到远处。有数据表明,每百万至千万个血细胞中才可能有一个CTC。因此,从血液中找到这些细胞的难度非常大,每毫升血液里面的CTC数量仅为个位数,相比之下白细胞的数量级是106-107——从大量血细胞中找到CTC,不比从四大名著中挑出几个错别字来得容易。
2.非典型形态
CTC的形状不规则,体积比血液细胞和正常组织细胞大;细胞核较大,形状不规则,核质比高。有的CTC是单个游离细胞,有的则聚集成团,形成循环肿瘤微栓子(CirculatingTumorMicroemboli,简称CTM),容易引发血栓栓塞。相比CTC,CTM更易免疫逃逸,避免失巢凋亡,生存力更强,放化疗耐受性更好,转移风险更高。临床研究显示,外周血中出现CTM的肿瘤患者,比只有CTC的患者,无进展生存期、总生存期更短。
3.异质性
CTC的异质性主要表现在:
(1)细胞表面抗原标志物表达差异很大,即使同一病人来源不同的CTC细胞所表达的标志物种类及表达量也有差异;
(2)不同的细胞携带不同的分子信息;
(3)不同的细胞转移潜力也不一样。
由于CTC试剂盒每次检测只能针对某几个靶点,单个芯片难以通用于检测不同分子信息的肿瘤细胞。因此,检测CTC时,试剂盒中的抗体种类和质量决定了CTC的捕捉率。抗体种类不足很容易导至假阴性检测结果。
《中国癌症杂志》2013年发表文章《循环肿瘤细胞在不同阶段不同类型乳腺癌中的应用》,讨论了CTC检测的临床应用。
1.CTC检测在转移性乳腺癌治疗中的应用
Cristofanilli等进行的前瞻性、多中心研究中,应用强生CellSearch技术检测177例转移性乳腺癌新一线治疗前、首次随访时的CTC状态,并且结合影像学检查评价疾病状态。结果显示:
CTC≥5个/7.5 mL外周血的患者无进展生存时间(progression-free survival,简称PFS)及总生存时间(overall survival,简称OS),短于CTC<5个/7.5 mL外周血的患者(2.7个月vs 7.0个月,P<0.001;10.1个月vs >18.0个月,P<0.001),首次随访时的数据也观察到一致结果;
经过治疗,CTC≥5个/每7.5 mL外周血的患者比例从49%降至30%,多变量COX比例回归分析表明,基线、首次随访时CTC数目是PFS以及OS的独立预测因素。
依此结果,2004年美国食品和药品管理局(FDA)批准了CellSearch检测系统应用于转移性乳腺癌预后评估。
江泽飞等进行的前瞻性、双盲、多中心大型临床研究(CBCSG004),第一次证实了CTC检测(CellSearch检测系统)在中国转移性乳腺癌中的应用价值。研究共纳入300例转移性乳腺癌患者,99例健康受试者及101例良性乳腺病患者,其中294例(平均年龄49.4±9.4岁,中位年龄50岁)可进行疗效评价。研究发现,对照组人群(健康受试者及良性乳腺病变者)CTC十分罕见,检出者不高于2个;294例转移性乳腺癌中,115例(39.1%)检出CTC≥5个(每7.5mL外周血),CTC水平与转移部位、激素受体状态及HER-2状态相关。研究证明了包括HER-2阳性、三阴性在内的各个亚型转移性乳腺癌中CTC检测(CellSearch检测系统)的预测价值。
2. CTC检测与影像学检查
与传统影像学检查方法比较的研究中,Liu等对74例转移性乳腺癌进行了CTC检测和影像学检查,其中68例允许CTC及影像学的联合评价,中位随访时间为13.3个月。研究表明:接受一线化疗及内分泌治疗的患者,其影像学评价,与基线CTC、影像学检查前3-5周、7-9周的CTC数目都具有相关性。治疗开始后3-5周CTC≥5个/每7.5mL外周血的患者,PFS更短,7-9周的差异未见统计学意义,但也可以看出PFS缩短的趋势。
Budd等共纳入177例转移性乳腺癌患者,其中138例符合入组条件。新的治疗开始前及治疗后10周分别进行CT检查,由2位独立影像科医师评估结果,同时在治疗后每4周采用CellSearch技术检测CTC。研究表明:
2位影像科医师的影像学评价变异率为15.2%,而不同实验室CTC评价的变异率仅为0.7%;
有13例(9%)患者影像学评价无疾病进展,而CTC≥5个/7.5 mL外周血,中位OS短于83例(60%)影像学评价无疾病进展且CTC<5个/7.5 mL外周血的患者(15.3个月vs 26.9个月,P=0.038 9);20例(14%)患者影像学评价为疾病进展且CTC<5个/7.5 mL外周血,中位OS长于22例(16%)影像学评价为疾病进展且CTC≥5个/7.5 mL外周血的患者(19.9个月vs 6.4个月,P=0.003 9)。
DeGiorgi等回顾分析了115例患者,比较治疗期间CTC与PET/CT对疾病的预测价值。研究表明:
如果治疗期间CTC≥5个/7.5mL外周血,CTC可以作为比较准确的评估预后的指标;
对于治疗期间CTC<5个/7.5 mL外周血的患者,PET/CT是一个更加有效的评估预后的工具;
CTC检测作为标准影像学检查手段之外的辅助评估方法,优势可能在于判断疾病进展,帮助患者及时调整治疗方案。
参考文献:
ASWORTH T R. A case of cancer in which cells similar tothose in tumors were seen in the blood after death [J]. AustMed J, 1869, 14: 146-149 .
GANGOPADHYAY S, NANDY A, HOR P, et al. Breast cancer stem cells: a novel therapeutic target [J]. Clin Breast Cancer, 2013, 13(1): 7-15.
黄红艳, 江泽飞. 循环肿瘤细胞在乳腺癌中的研究进展[J]. 国际肿瘤学杂志, 2011, 38(7): 516-518.
MOSTERT B, SLEIJFER S, FOEKENS J A, et al. Circulating tumor cells (CTCs): detection methods and their clinical relevance in breast cancer [J]. Cancer Treat Rev, 2009,35(5): 463-474.
DAWOOD S,CRISTOFANILLI M.Integrating circulating tumor cell assays into the management of breast cancer [J].Curt Treat Options Oncel, 2007, 8(1): 89-95.
CRISTOFANILLI M, BUDD G T, ELLIS M J, et al. Circulating tumor cells, disease progression, and survival in metastatic breast cancer [J]. N Engl J Med, 2004, 351(8): 781-791.
GIORDANO A, GIULIANO M, DE LAURENTIIS M, et al. Circulating tumor cells in immunohistochemical subtypes of metastatic breast cancer: lack of prediction in HER2-positive disease treated with targeted therapy [J]. Ann Oncol, 2012,23(5): 1144-1150.
JIANG Z F, CRISTOFANILLI M, SHAO Z M, et al. Circulating tumor cells predict progression-free and overall survival in Chinese patients with metastatic breast cancer, HER2-positive or triple-negative (CBCSG004): a multicenter, double-blind, prospective trial [J]. Ann Oncol, 2013. [Epub ahead of print]
BUDD G T, CRISTOFANILLI M, ELLIS M J, et al. Circulating tumor cells versus imaging--predicting overall survival in metastatic breast cancer [J]. Clin Cancer Res, 2006, 12(21): 6403-6409.
DE GIORGI U, VALERO V, ROHREN E, et al. Circulating tumor cells and [18F]fluorodeoxyglucose positron emission tomography/computed tomography for outcome prediction in metastatic breast cancer [J]. J Clin Oncol, 2009, 27(20): 3303-3311.
 /3
/3 