拿到CFDA创新医疗器械特别审批的时候,飞朔生物正式运营还不到两年。 飞朔生物是位于厦门的一家生物技术企业,致力于为肿瘤精准医学检测提供产品和服务。公司的“基因测序用文库试剂盒”为国内首个获得一类医疗器械备案证产品。另外,公司有5个产品获得国际欧盟CE-IVD认证,多个产品正在申请国家食品药品监督管理局三类医疗器械注册证。 CFDA从2016年下半年开始向NGS肿瘤临床检测行业释放利好消息,一时间,行业内所有人的神经都紧绷起来。这么大一个市场,尚未有一家企业NGS肿瘤产品获得CFDA的批准认证。 无疑,谁率先拿到通行证,谁就能够占据先发优势。网站、公众号转载请联系动脉网。 几乎所有企业都争先恐后的开始进行、或着手准备肿瘤诊断试剂盒产品的申报。而这家行业内知名度并不高,2016年才成立的企业,却成为第五家拿到特别审批的企业。 对许多人而言,他们好像半路杀出的程咬金。
2012年,在艾德生物做了6年多的研发、生产和市场工作后,陈琰进入赛默飞世尔(Lifetech)开始接触NGS产品的临床转化工作。当时他负责的是一代测序、二代测序产品、实时荧光PCR和数字PCR产品的临床应用市场。 肿瘤领域是他当时工作的重心,美国总部也很重视。 在艾德生物的几年,让他积累了许多分子病理医生资源。在与这些临床专家的交流中,得到反馈:1.多基因联合检测成为临床应用的新需求;2.需要更加操作简单、快捷的方法。而此时,NGS正在往肿瘤领域扩展。 他隐约觉得这项技术有可能为临床肿瘤检测带来新的变革:“现有荧光PCR技术对实行多基因检测时时间太长了,肿瘤病人不一定等得起。” 之前做过研发工作,带着这样的思路,一次偶然的机会,陈琰有了新的想法,这便是飞朔生物的核心专利环介链接扩增技术(RingCap)。 当时NGS在IVD行业的应用已经相当广泛,临床监管也到了临界点。2015年下半年,陈琰开始有了创业的想法。
2015年12月31日,陈琰正式离开赛默飞世尔;2016年1月1日,飞朔生物正式运营。 2015年的十月份,跟一位企业家沟通时,当下便同意天使轮投资该项目,厂房和办公区也租下来了。直到一月份正式运营,公司从上到下也就陈琰一个人。装电话线、装宽带、买电脑,这些全都是陈琰自己去搞定。直到2月份自己的太太加入,公司才算有了第一个核心成员。 “我太太在艾德生物负责了8年的质量管理体系工作,怎么建质量管理体系、怎么管理、怎么报证,这些她都非常专业。”陈琰告诉动脉网。
成立之后,飞朔生物如同它的名字一样,飞速发展。 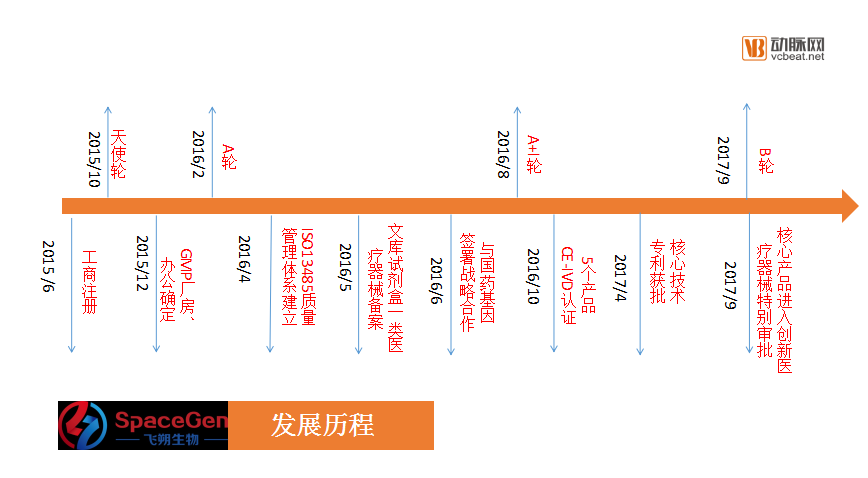 2016年2月拿到乔景资本千万级A轮融资;4月完成质量管理体系建立;5月便拿到了基因测序用文库试剂盒一类医疗器械备案,他们是全国国内第一家。2016年10月,公司完成5个产品的欧盟CE-IVD认证,这些产品具备了在欧盟成员国地区的销售资质。 肿瘤临床检测未来市场可能达到200亿,这是一个非常大的市场,也是个竞争激烈的市场。 “这个市场大约能够允许容纳十几家企业,而目前这个市场的企业有数百家。”陈琰表示。 飞朔生物成立的时候,整个基因检测领域已经爆发过一次融资潮。竞争对手已经多,他们成立的不算早。要在数百家企业中脱颖而出,唯快不破。
目前团队规模超过50人,研发团队成员占据1/3,而销售团队还不到10个人。 相比大范围的去医院收样做第三方检测,陈琰更倾向在这个阶段把精力放到产品申报和开发上。 首先,目前试剂盒产品的申报本就已经进入一个微妙的阶段。谁能够率先拿到CFDA的通行证,谁就能掌握先机。 但这个优势持续时间并不会太长。进入市场后,一号选手需要在短时间内迅速与医院建立紧密的关系。如果一号选手把市场内所有医院都拿下来的话,第二家、第三家企业就没有那么容易了。 肿瘤市场足够大,第二家、第三家企业还可能在第一家的手中分到一定市场。但越后进入市场的企业一定会走的越困难,先发优势尤为重要。 因此,作为一家成立并不算早的企业,与其在现阶段大规模扩张市场团队,不如把更多的精力放在产品开发和研发上,尽可能成为进入市场的第一批企业。 “我们是试剂盒的生产供应商,目前会把更多的精力放在产品的研发上,所以现阶段一个销售人员需要覆盖多家医院甚至一个省。”陈琰这样告诉记者。公司在2016年一整年都没有销售活动,全部尽力都集中在产品研发、生产、性能验证和资质申报上。在他看来,IVD行业中,资质和技术才是第一位。 到目前为止,飞朔生物的试剂盒产品已超过30个。 2017年9月,公司核心产品肿瘤诊断试剂盒产品进入国家医疗器械特别审批程序。公司是第五家拿到肿瘤试剂盒特别审批的企业,而最先获批的几家企业,早在2015年就提交了申请。CFDA今年8月初才明确了二代测序技术肿瘤伴随诊断试剂盒申报的指导评价原则,目前大家处于同一起跑线上。 “在注册申报上,我们的投资方达瑞生物也给了我们很多帮助。”陈琰表示。
公司给自己的定位是上游的试剂耗材生产供应商。陈琰认为,如果单单只是做一个第三方检验所,那企业密度非常大,竞争也比较激烈。而如果作为上游的供应商,下游的竞争在一定程度上反而能够促进企业发展。 而作为上游企业,有两点是非常重要的:一是产品的技术,是否能够在业内保持优势、是否能够符合市场需求;另外则是合法合规,拿到监管部门的审批。 飞朔生物在2017年4月拿到了国家知识产权局授权的核心技术专利。而在产品的开发上,飞朔生物选择与临床专家合作,开发出更符合临床实际需求的产品。
除了向市场提供治疗体系标准的产品以外,飞朔生物还面向医院提供定制化的服务。 “临床专家可能针对不同的癌症有新的研究,这些研究如果要发表文献需要试验数据的支持,我们就可以与他们合作,把想法做成产品。”陈琰介绍到。在公司的支持下,医生可以基于这些数据和产品进行专利申报,飞朔则又可以通过专利授权的方式进行新产品的开发转化。 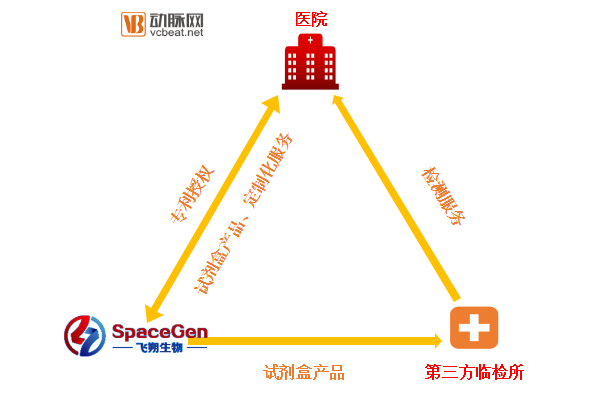 “这样的话我们就有了一批活跃的智库,产品也能够源源不断的输出。”陈琰表示。
随着第一个肿瘤试剂盒产品进入特别审批,几乎市场上所有企业都开始着手或者准备试剂盒产品的申报工作。在第一个产品获批后,一定会有更多的企业陆续拿到审批。也就是说,在第一个产品进入市场后,市场竞争将在一段时间内迅速增加。 随着时间的推移,竞争会越来越激烈。而那个时候,市场竞争已经不单单是技术或者渠道竞争,而是综合实力的较量。除了在产品开发上投入大量精力外,飞朔生物在渠道竞争上也早有布局。 2016年6月,飞朔生物与国药基因签署了战略合作。国药集团是由国务院国资委直接管辖的中国规模最大、产业链最全的医药健康产业集团。物流分销一体化、配送网络是国药集团正在全力推经的平台之一,覆盖医院超过3万多家。 双方将合作加速飞朔生物肿瘤基因突变检测系列产品的产业化,未来也将为产品的渠道和配送提供支持。 公司在2017年9月获得了由景旭创投、景圆蓝海和东方翌睿共同参与的B轮融资,不到两年时间,公司已陆续完成了四轮融资。  下一步,公司将持续把精力放在产品上,保持每年3-5个产品拿到审批认证。肿瘤试剂盒的审批流程是重中之重,他们希望能够成为进入市场的第一批企业。 同时公司将尝试把更多的新技术向临床转化,紧跟海外市场,做出更符合临床需求的产品。 |
 /3
/3 