2018年11月2日,国家药品监督管理局发布《创新医疗器械特别审查程序》,新修订的《创新医疗器械特别审查程序》自2018年12月1日起施行,原试行规定将同时废止。
为鼓励医疗器械的研究与创新,促进医疗器械新技术的推广和应用,推动医疗器械产业高质量发展,我国于2014年3月1日起施行《创新医疗器械特别审批程序(试行)》。符合条件的医疗器械注册申请人可以向药品监管部门申请以特别审批程序进行审批。在审批程序的诸多环节中按照早期介入、专人负责、科学审批的原则,对创新医疗器械予以优先办理,从而加快其审批进程,并加强与申请人的沟通交流。此制度是“加快上市审评审批”是重要改革措施之一,审批比例呈现逐年递增的趋势。截止2018年10月30日,已有196项产品通过了特别审批程序,其中IVD产品43项,占比21.94%。
2014年-2018年10月通过创新医疗器械特别审批持续的产品数量
小编整理了通过创新医械特审的34家国内IVD企业的研究动向,以供大家阅读参考。
从整理的资料可以看出,申报的创新体外诊断产品以分子诊断领域为主。基因测序的巨大市场前景也吸引了大量的企业与资本,据统计,2017年,中国基因测序行业共披露融资60次,明确披露融资金额的27笔,2017年融资总金额超过68亿人民币,单笔融资金额超过亿元人民币的有19笔。
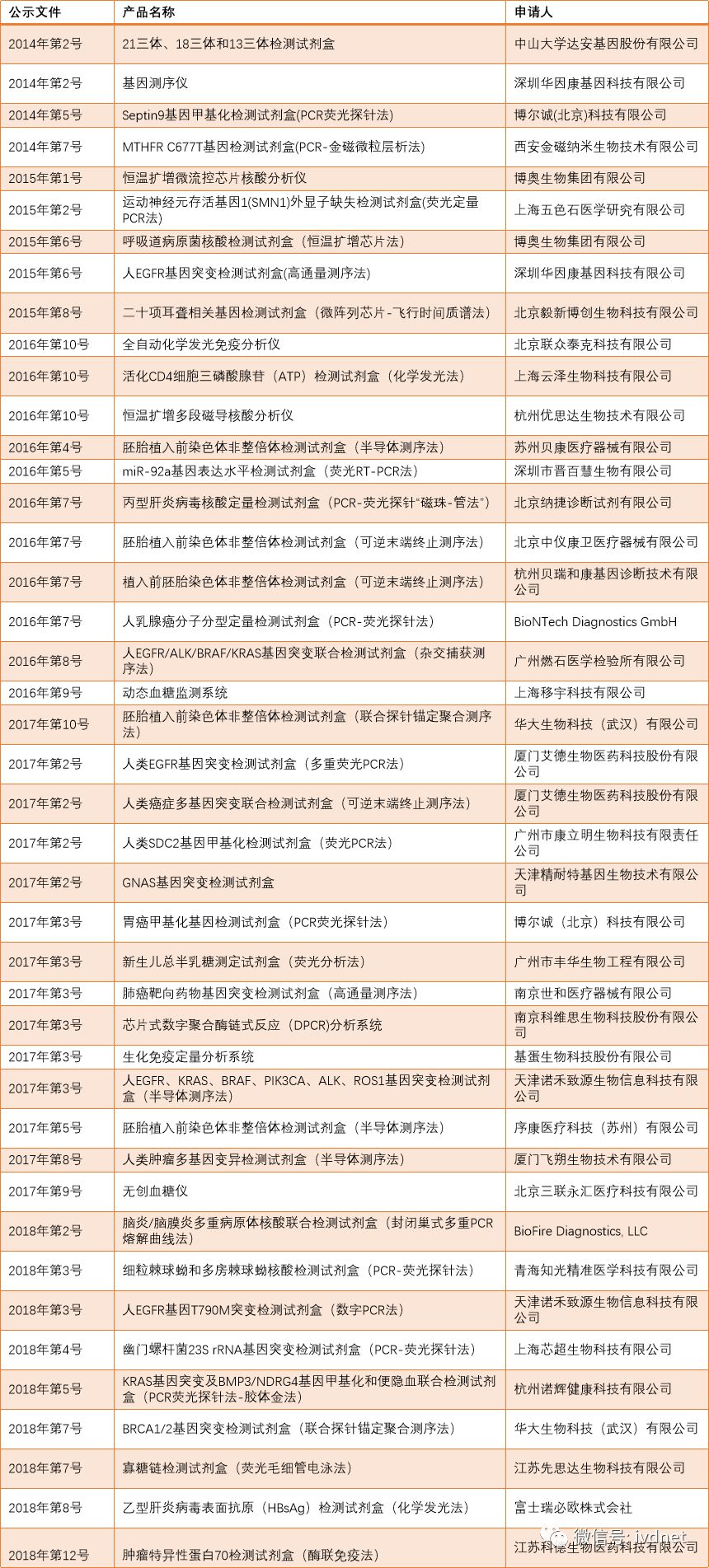
附:全部IVD领域创新产品清单













 /3
/3 





 浙公网安备33010802005999号
浙公网安备33010802005999号


