图 :ctDNA 检测原理
ctDNA(circulating tumor DNA,循环肿瘤DNA)是指人体血液循环系统中不断流动的携带一定特征(包括突变,缺少,插入,重排,拷贝数异常,甲基化等)来自肿瘤基因组的DNA 片段。ctDNA 的主要来源包括来源:1、来自坏死的肿瘤细胞;2、来自凋亡的肿瘤细胞;3、循环肿瘤细胞;4、来自肿瘤细胞分泌的外排体。传统的组织活检必须要知道肿块的位臵,这就让我们很难做到对肿瘤的早期预防。但如果肿瘤的碎片进入到血液里面去,我们从血液当中检测出来,在影像可见的阶段之前,让我们提早预测到组织肿块,这就能比传统的诊断获得更早的机遇,抓住更好的治疗机会。非侵入性液体活检可以提前发现癌症的高危群体,提早对肿瘤的发展进行干预。理论上讲,一个细胞含有约6-7pg 的DNA,1mL 血能提取10ng 游离DNA,相当于来自约2000-3000 个凋亡细胞的DNA 量。但是一般情况下只占整个循环DNA 的1%,甚至只有0.01%。因此,这对DNA 的检测技术提出了比较高的要求,目前,ctDNA 检测的主要技术手段包括:BEAMing、数字PCR、ARMS-PCR,TAM-Seq、CAPP-Seq,NGS等。对ctDNA 的分析包括定性和定量的分析,其中定性分析包括检测基因突变、缺失、插入、融合、重排、拷贝数变异、甲基化、微卫星不稳定(MSI)和杂合性缺失(LOH)等;定量分析就是计算ctDNA 在血液中实时的含量。定性和定量两种方法均可以反映肿瘤的存在和严重程度。
◆ ◆ ◆ ◆ ◆ ctDNA 的发展历程 图 :ctDNA 发展历程
>>1948 年,发现ctDNA。Mandel 和Metais 发现血浆中存在游离的核酸分子(CR Acad. Sci. Paris 142, 241–243,1948),不幸的的是由于当时对血液中循环DNA 分子缺乏理解,这项研究并未引起重视。在此之后的30 年中,仅有两篇关于自身免疫病的文章报道了ctDNA(J. Clin. Invest. 45, 1732–1740,1966; J. Clin. Invest. 30, 1732–1740,1951)。>>1977 年,发现ctDNA 与肿瘤存在相关性。肿瘤患者的血浆游离DNA 水平要明显高于健康人群,在化疗之后ctDNA的水平会降低(Cancer Res. 37, 646–650,1997);>>1994 年,肿瘤中的标志性基因突变在ctDNA 中也存在。胰腺癌患者的ctDNA 含有胰腺癌的标志性基因K-Ras 的突变(Cancer Epidemiol. Biomar. Prev. 3, 67–71, 1994);同年,骨髓增生异常综合征的标志性突变N-ras 也在ctDNA中被报道(Br. J. Haematol. 86, 774–779, 1994)。>>1996 年,ctDNA 的的微卫星序列在肿瘤病人血液中被发现。在此之后的几年里很多cfNA(cell free nuclear acid,包括DNA,mRNA 和micro-RNAs)纷纷被报道(Nat Med, 2:1035–1037.1996)。>>1997-1999 年,cfDNA 中的突变与多种肿瘤的相关性相继被报道。(Gastroenterology,112:1114–1120,1997.;Br JCancer,80:1262–1264. 1999)>>2008 年,ctDNA 与疾病监测。结肠癌中APC 的突变的动态变化被用来检测肿瘤病人的疾病发展状态。(NatMed,14:985–990, 2008)>>2009 年,EGFR T790M 的突变在肺癌病人中被发现,并用于指导用药。(Clin Cancer Res,15:2630–2636,2009)>>2012 年,ctDNA 与耐药性研究。第一例获得性耐药的机制在结直肠癌病人中被发现。>>2013 年,ctDNA 全外显子测序被用于病人的耐药性研究中。(Nature, 497:108–112,2013)>>2016 年,FDA 批准Epigenomics 公司以血液为基础筛查大肠癌的Epi proColon 技术,这是目前第一个被FDA 批准的ctDNA 检测产品。代表着政策开始向ctDNA 检测开放。
◆ ◆ ◆ ◆ ◆ ctDNA 的富集
图 :ctDNA 富集方法
血液中含有大量游离在细胞外的核酸(cfDNA),不仅包括来自肿瘤的核酸(ctDNA),还包括其他来源的核酸。在检测ctDNA 的第一步就是将cfDNA 从血液中抽提出来。由于ctDNA 浓度低而且高度碎片化,富集和分离就显得尤为重要。一般我们需要5-10mL 血液,收集后,取血清或血浆分离cfDNA。血液经抗凝处理后的全部血液为全血;离心除去血细胞后所得到的淡黄色液体为血浆。血液不经抗凝处理,自行凝固后,血液除凝固的部分以外的清澈淡黄色的液体就是血清。虽然血清中ctDNA 的浓度是血浆中的3-24 倍,但是凝血过程中容易产生的杂质污染。相比之下,用血浆提取DNA 使用更广泛。由于血液中DNA 酶的存在,使得cfDNA 在血液中不稳定,易被降解。分离DNA 应在抽血后的数小时内完成。常用于分离ctDNA 的方法有两种:>>离心柱法 以硅胶滤膜作为固相载体的,基于二氧化硅选择性结合DNA 的独特属性。其原理是带负电的DNA骨架与带正电的硅胶滤膜之间的高亲和力。钠离子起到阳离子桥的作用,它可以吸引核酸磷酸骨架里带负电荷的氧。在高盐条件(pH≦7)下,钠离子可破坏水中的氢与硅中带负电荷的氧之间的氢键。通过大量漂洗去掉所有杂物后,用TE 或Tris-Hcl 缓冲液或蒸馏水在低离子强度下(pH≧7)洗脱纯化的DNA。>>磁珠法 带有磁荷的颗粒可通过磁场中的永磁将其移除。这些磁颗粒可用表面包被活性基团的氧化铁颗粒制成。因表面积大,结合核酸的能力较强,可作为较好的分离载体。如果赋予容器侧壁磁性,样品混合物中结合有核酸的磁珠则聚集到容器壁,直接倾倒容器可将其他杂质去除,避免了反复离心。磁珠表面包被有活性基团可特异性吸附核酸。磁珠分离技术是现今核酸纯化的一种简单快速的方法。表 :游离核酸的常用提取方法比较 cfDNA 检测一般采用虑柱法,因为提取效率高,而且cfDNA 测序所需的外周血量大,一般为5mL-10mL;磁珠法可以用于NIPT 的检测,因为母体中胎儿游离的DNA 量比较丰富,可以达到母体外周血中cfDNA 总量的10%,磁珠法的优势是简单快速。目前来看,分离和富集血液中的cfDNA 并不是瓶颈,市面上有很成熟的试剂盒可以抽提得到足量的cfDNA。瓶颈主要在于之后的ctDNA 的检测与分析。
◆ ◆ ◆ ◆ ◆ ctDNA 的检测方法 图 :ctDNA 检测技术发展趋势
桑格测序和焦磷酸测序法是最早,最成熟的DNA 测序手段,但由于灵敏度较低,不能检测血液中微量的DNA,在液态活检中没有应用价值。ctDNA 检测技术中使用最广泛的是dPCR 和ARMS,由于其成本低,灵敏度高,适合检测血液中微量的DNA。目前有多种基于dPCR 或ARMS 设计的实验技术,在dPCR 或ARMS 的基础上提高了灵敏度和准确度。但是依然无法克服dPCR 或ARMS 的缺点:低通量,不能检测未知突变。二代测序技术(NGS)能够很好的弥补dPCR 在ctDNA 检测上的不足,但缺点是价格太高,目前难以在市场推广。为了在保证检测准确性和测序深度的基础上降低价格,目前越来越多的新技术关注于ctDNA 目的片段的富集。将富集后的目的序列进行深度测序,能够很好的保证高通量检测多个已知和未知的突变,同时控制成本。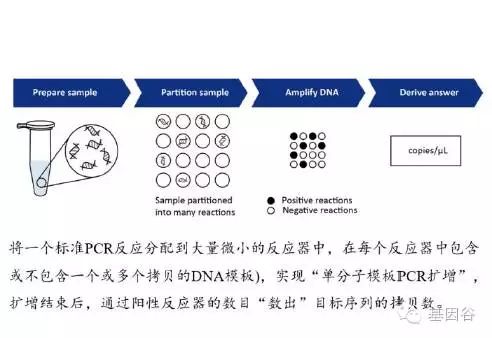 图 :液滴数字PCR(ddPCR)简介
图 :BEAMing 技术 1) 液滴数字PCR(ddPCR) 将一个标准PCR 反应分配到大量微小的反应器中,在每个反应器中包含或不包含一个或多个拷贝的目标分子(DNA 模板),实现“单分子模板PCR 扩增”,扩增结束后,通过阳性反应器的数目判断目标序列的拷贝数。2) BEAMing 结合数字PCR 与流式技术,通过磁珠克隆DNA。利用特异性PCR 引物扩增目标突变区后,与磁珠(磁珠上固定有特异的PCR 引物)混合进行油包水单分子扩增反应。反乳化作用后,利用不同颜色的荧光探针结合磁珠上的PCR 产物,发出红色或绿色荧光。使用流式细胞仪分析磁珠颜色来确定突变情况。图 :ARMS-PCR 技术简介 3) ARMS-PCR 全称amplification refractory mutation system,扩增受阻突变体系。是一种在PCR 基础上发展起来用于检测DNA 中各种点突变的新方法。其依据的基本原理是:TaqDNA 聚合酶缺少3′→5′外切酶活性,因此对于3′末端错配的引物,以低于正常末端配对引物的速度延伸,当错配碱基的数目达到一定程度或者条件达到一定的严谨程度时,3′末端碱基则因磷酸二酯键形成困难。不能延伸,反应终止,也就得不到特异长度的扩增条带,从而表明模板DNA 没有与引物3′末端相应的突变;如果PCR 结果能得到特异长度的扩增条带,表明模板DNA 上具有与引物3′末端相应的突变。表 :已知基因突变检测方法的灵敏度对比(肺癌EGFR 基因) 2015 年12 月Lung Cancer 上发表了Kenneth S. Thress 等人关于EGFR 不同突变不同方法的比较,所有突变都是已知突变。文中比较了4 种给予DPCR 的检测方法,分别是cobas,ARMS-PCR,ddPCR 和BEAMing dPCR。从文中我们可以看出这三种方法各有优劣,在T790M 的突变上,ddPCR>BEAMing dPCR> ARMS-PCR >cobas.在19 位外显子缺失上,ddPCR 不能检测,而BEAMing dPCR >cobas> ARMS-PCR。在L858R 突变上,ddPCR=cobas >BEAMing dPCR>ARMS-PCR 。我们可以发现,各种方法在检测上各有优劣,不同的突变类型适合不同的方法。利用上述方法检测已知位点的突变在肿瘤个性化用药指导中现在已经有很广泛的应用。然而,在肿瘤中已知突变类型的肿瘤是很少的。大部分肿瘤的突变都是未知的。这就需要我们更好的方法去检测这些未知突变。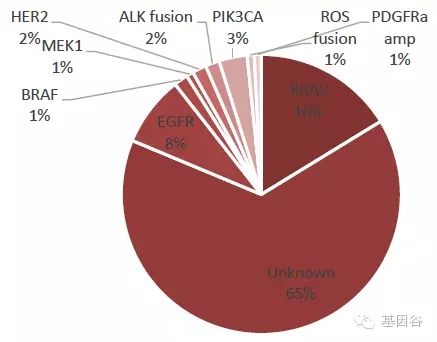
图 :肺腺癌的突变类型及比例图 :肺癌个性化用药策略 前面提到的几种技术虽然准确率高,成本低,但是通量低,不能检测未知突变,未来发展能力有限。以肺腺癌为例,我们可以看到大部分肺腺癌的突变类型我们都是不知道的。最大类的两个突变KRAS 和EGFR 分别占了16%和8%,有65%的突变是未知的。这就需要我们结合能够检测未知序列的方法来判断这些肿瘤病人的突变类型,实现肿瘤病人的精准用药。测序本身没有技术瓶颈,关键在于目的DNA 的靶向富集。下面我们主要介绍两种最新的联合DNA靶向扩增和测序的方法,分别是TAM-Seq 和CAPP-Seq。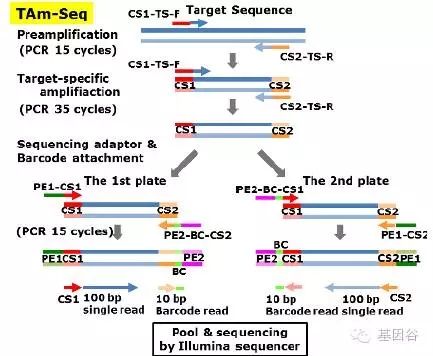
图 :标记扩增深度测序(TAM-Seq)
图 :癌症个体化深度测序 (CAPP-Seq) 4) TAM-Seq tagged-amplicon deep sequencing,即标记扩增深度测序法。该方法的基本原理是设计特异性引物对目标区域进行循环预扩增,产生大小200bp 以下末端重叠覆盖整个区域的扩增子(预扩增),接着通过单重PCR选择性扩增带突变的扩增子区(标签扩增),从而排除非特异性产物,最后在回收的产物上加接头和特异性条形码,进一步通过单端测序得到最终结果。5) CAPP-Seq 深度测序肿瘤个体化建档法,Cancer personalized profiling by deep sequencing。CAPP-Seq 法先在在肿瘤基因突变数据库(COSMIC,“筛选库”)来源寻找重复出现的突变相关的外显子,再从肿瘤基因图谱库的407位NSCLC 患者全基因组测序结果筛选突变,设计探针,靶向富集含139 个常见突变基因中的521 个外显子和12个内含子,长度约为125kb,有效的把测序区段浓缩到整个基因组大小的0.004%,使得后续超高深度测序得以实现。其对肿瘤的ctDNA 检测灵敏度更高,特异性更强,与全外显子测序等相比经济可行。从ctDNA 的技术发展路线我们可以看到,ctDNA 在向着高精度和高通量的方向发展。NGS(下一代测序)虽然可以做到高通量,并且能够检测未知序列,但是全外显子组测序成本太高,难以在疾病市场推广,未来主要还是用于研发。所以最新的研究都集中在富集靶向DNA,将富集后的DNA 拿去做超深度测序可以大幅降低成本(CAP-seq 可以将目的序列浓缩到原整个基因组大小的0.004%)。但是,如何高效准确的富集目的DNA 序列是目前ctDNA 检测的瓶颈。
◆ ◆ ◆ ◆ ◆ ctDNA 测序方法精度比较 表 :ctDNA 检测灵敏度临床研究结果
我们整理分析的近年来关于相关ctDNA 临床研究的论文。上图展示了不同方法对于不同癌症不同时期的检测准确率情况。从目前的研究来看,ctDNA 对于早期癌症(原位癌和I 期临床病人)的检测准确率很低,例如膀胱癌原位癌准确率约为57%,胰腺癌原位癌准确率约为50%,结直肠癌I 期准确率仅仅为37%。相比之下,对于晚期肿瘤(IV期)的准确率非常高,大部分都能超过80%的准确率,有一些癌症甚至能达到100%。从临床数据可以看出来,通过ctDNA 进行肿瘤的早期筛查依然很困难,这与肿瘤早期血液中ctDNA 含量少,难以检测有关。不同时期,癌症患者特内的ctDNA 含量不同。在癌症后期,由于ctDNA 含量多,检测难度低。所以,在癌症治疗市场,其瓶颈在于如何低价高效的全面的覆盖肿瘤的各个突变。在保证准确率的基础上降低检测成本,是液态活检在癌症治疗领域应用的关键,大规模的临床实验有助于行业标准的建立。例如:Foundation Medicine 的 FoundationOneHeme 检测405 个癌症相关基因,FoundationACT 检测62 种基因突变和6 种融合基因,FoundationOne 检测315 个癌症相关基因;世和基因的体外诊断产品血递安检测416 个相关基因。目前这些产品价格大都在10000 元以上,难以大规模推广,检测成本是这个环节的瓶颈所在。在肿瘤早期筛查市场,由于肿瘤早期ctDNA 含量少,需要先富集目的序列再进行深度测序。对DNA 进行深度测序并不存在技术难度,市面上有成熟的仪器和方法进行检测。通过ctDNA 进行的癌症早期筛查瓶颈主要在于高效的靶向扩增和数据分析,其中最关键的是目的基因的靶向富集技术。我们认为,具有靶基因富集技术,大量临床样本和大数据分析能力的公司未来将在ctDNA 早期癌症筛查能力最先突破。
|



 /3
/3 