手摇式数字液滴LAMP技术用于病毒载量的定量即时检测
2024-2-23 16:36|
发布者: 沙糖桔|
查看: 3375|
评论: 0|来源: 老和山下说IVD
摘要: 现有的病毒载量检测技术主要包括斑点试验和核酸扩增反应。

病毒载量的定量检测在临床传染病诊断、传染风险评估、患者治疗监测等领域具有重要的作用。现有的病毒载量检测技术主要包括斑点试验和核酸扩增反应。其中,斑点试验可直观反映病毒载量和活力的相关信息,但步骤繁琐、反应周期长,无法在即时检测中发挥应有的作用。以qPCR为代表的核酸扩增技术,具有定量准确、反应速度快(<2 h)、灵敏度高(~100 CPs/mL)等优势,但却依赖于专业设备与操作,且需要借助标准曲线进行定量检测。相比之下数字液滴PCR(ddPCR)技术可在不需要标准曲线的情况下实现目标病毒的绝对定量,因而在低浓度下准确性更高。然而ddPCR设备复杂,甚至比qPCR更加昂贵,因此应用场景受限于医院或中心实验室。针对上述问题,加利福尼亚大学的Adam
R. Abate课题组开发了一种手摇式液滴生成技术,与环介导等温扩增技术(LAMP)相结合,构建了一种操作简便、无需大型仪器的病毒载量即时检测新方法(Shaken
digital droplet reverse transcription-LAMP,sdd RT-LAMP),并用于SARS-CoV-2的定量检测。sddRT-LAMP基本检测流程 sddRT-LAMP的基本检测流程如图1所示,首先从患者处采集样本(图1a)并存储于转运缓冲液中,样本可以冷冻保存以供后续分析,或立即进行检测。将待测样本与提取缓冲液混合并裂解5 min,加入RT-LAMP反应预混液和封装油后(图1b),将反应管快速摇晃30
s,以形成多分散的乳化液滴(图1c)。于65 ℃恒温反应30 min,包含目标病毒的阳性液滴将产生显著的荧光信号,而阴性液滴则没有荧光产生。为实现定量检测,该论文中还设计了一种便携式的荧光成像装置,其成像腔室包含一个浅区域(80微米)用于单层成像,一个深区域(190微米)用于多层成像。最终利用智能手机对成像区域进行拍摄分析,即可根据荧光液滴的数量实现对目标病毒载量的即时检测。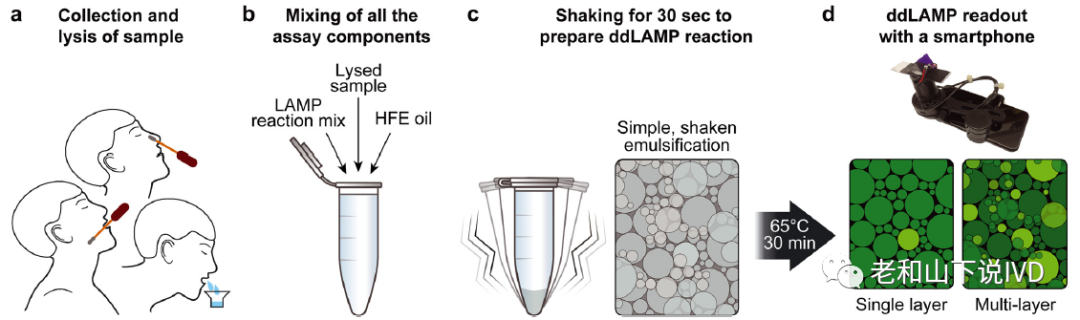
图1. sddRT-LAMP基本检测流程
摇晃乳化法用于病毒载量定量检测 基于上述检测原理,该论文设计了靶向识别SARS-CoV-2核衣壳蛋白目的基因(图2a)的引物与荧光探针,建立了一种针对于SARS-CoV-2病毒载量的定量检测技术。将待测样品和反应预混液通过手工摇晃约30秒,从而与含有表面活性剂的油乳化,生成pL级别的液滴,其中部分液滴包裹了单个目标分子。所得的多分散乳化液滴的平均粒径约为15微米(图2b,蓝色),因此20 μL的反应体系可生成约1000万个液滴。由于多分散液滴体积与直径的立方关系,大液滴尽管很少见,却包含了相当大的样本体积(图2b,橙色)。但即便液滴是多分散的,≥70%的样本体积被封装在直径≤65微米的液滴中,因此在适当的样本浓度下可以忽略液滴的多分散性来进行病毒载量的评估(图2b,红色虚线)。为了确认摇晃乳化法用于液滴生成的有效性,该论文将sddRT-LAMP技术与qPCR技术进行了比较。将待测样本梯度稀释至2.68~2680
CPs/reaction(536~536000CPs/mL),并用两种方法分别进行了分析,检测结果展现出良好的一致性(图2c)。这些结果表明,sddRT-LAMP具备与qPCR相当的定量准确性,且从便携性上更适用于病毒载量的即时检测。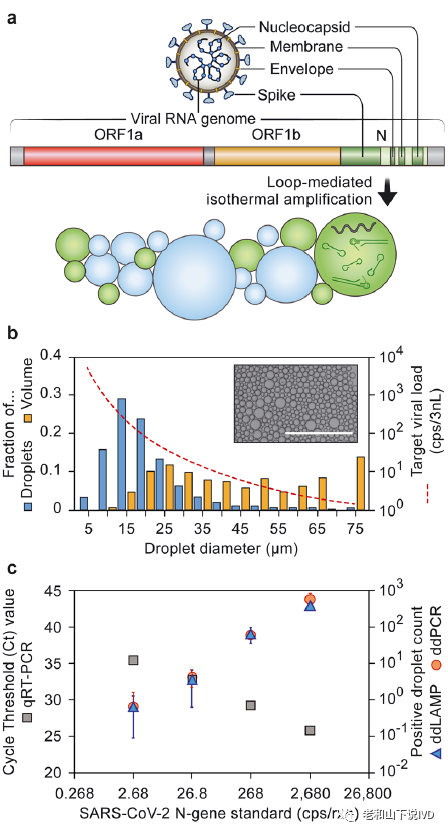
图2. 摇晃乳化法用于SARS-CoV-2病毒载量定量检测
便携式成像装置实现更广的动态范围 为了使用液滴计数实现精确的目标定量,该论文开发了一种手持式的成像腔室,其装载方便,能够在单个视野中容纳整个20
μL反应体系,针对病毒载量的动态检测范围覆盖了3个数量级(图3a)。其成像腔室包含一个浅区域(80微米)用于单层成像,一个深区域(190微米)用于多层成像。当病毒浓度较低(<10 CPs)时,阳性液滴很少,因此即使在多层区域中也往往是独立存在的,可以逐个计数(图3c)。而当病毒浓度较高(>100 CPs)时,阳性液滴较为普遍,并且倾向于在多层区域中重叠,不利于定量的准确性。此时浅区域更倾向于形成单液滴层,使其能够清晰得分辨阳性液滴的数量(图3d)。因此,这种双层高成像腔室提供了一种简单的方法,可以在更广泛的靶标浓度范围内获得准确的测量结果。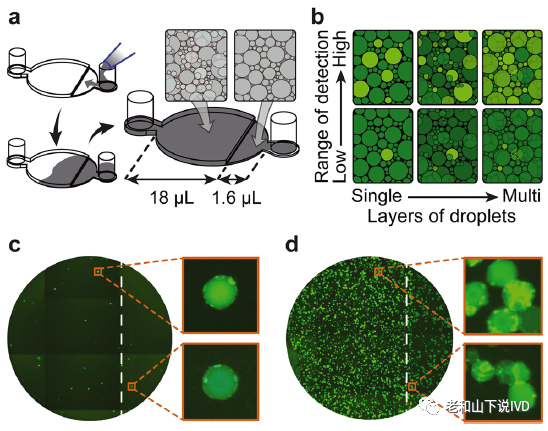
图3. 便携式成像装置实现更广的动态范围
智能手机实现液滴成像和计数 智能手机配备了高灵敏度和高分辨率的摄像头,结合廉价的商用硬件,即可作为便携式的荧光显微镜使用。为了验证这种设备进行液滴定量的可行性,该论文设计了一个安装在智能手机上的光学系统(图4a)。该系统的外接硬件包括用于高分辨率成像的10×目物镜,荧光的激发光源和电源。样品腔室被放置在成像平台上,启动照明,然后由摄像头拍摄图像(图4b)。为了确定该设备的成像效果,将其与实验室荧光显微镜进行了对比。如图4c所示,智能手机图像的质量较差,光背景更高,分辨率总体较低,但尽管如此,阳性液滴仍然可在多层和单分子层区域中被观察到,从而证明了液滴计数的可行性。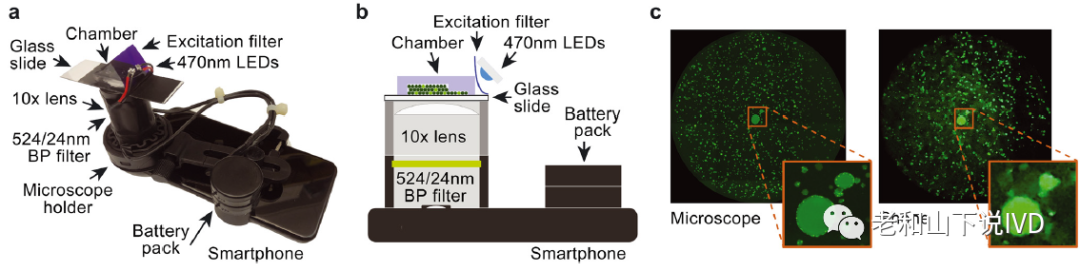
图4. 智能手机实现液滴成像和计数
临床应用价值评估 为了验证该装置用于病毒载量即时检测的临床应用价值,该论文分析了2020年至2021年间收集的111个来自于加利福尼亚大学旧金山分校(UCSF)临床微生物学实验室的患者样本。由于Alpha(B.1.1.7)是该时间内主要流行的SARS-CoV-2变异株,因此检测所使用的引物和探针专门针对该变异株设计。利用sddRT-LAMP技术分析了病毒载量在1~5000 CPs/reaction(200~1000000 CPs/mL)范围内的样本,检测结果表明低浓度样本产生了很少的阳性液滴(图5a),而中等和高滴度产生了相应比例的阳性液滴(图5b和c)。阴性对照则未观察到阳性液滴(图5d),反映了该检测体系良好的特异性。双层高成像腔室对于阳性液滴的统计结果证明了该方法在增加动态范围方面的有效性(图5e)。由于智能手机分辨率不如荧光显微镜,且背景较高,它往往会错判或漏判阳性液滴的数量,二者相关性斜率仅为0.56(图5f),但相关系数较高(约0.98)。该结果表明虽然手机检测到的阳性液滴大约只有实际数量的一半,但它能够准确定量样本(图5g)。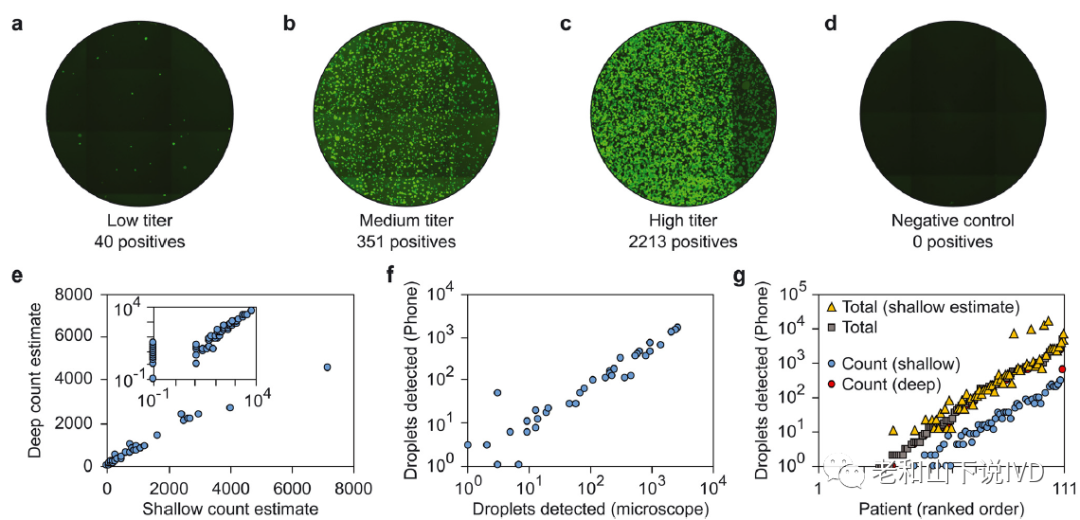
图5. 临床应用价值评估 该论文构建了一种设计简单、无需大型设备的装置用于病毒载量的定量检测。通过对100多个新冠患者样本的分析,该方法展现出较广的动态检测范围(3个数量级),且准确性与qPCR相当。该装置具备进行核酸POCT的潜力,但仍然具有较大的改进空间。液滴的生成与扩增产物的转移需要人工进行操作,用户的主观因素会对检测结果造成较大的影响,因此在自动化上需要进行提高。该装置暂未将样本处理、核酸扩增、信号转导与输出等多个检测环节进行集成。通过微流控芯片设计的进一步优化,构建一体化的反应腔体,有望进一步提高用户友好度和安全性。此外,基于液滴的微流控检测技术可与荧光多重检测相结合,从而实现多重核酸靶标的定量检测,利用单个反应体系即可完成多种病毒或某一病毒多种变异株的精准检测。[1] Viral load quantitation at the point-of-care with shaken
digital droplet RT-LAMP. Lab on a Chip, 2023,
23, 3479-3486.
|
声明:
1、凡本网注明“来源:小桔灯网”的所有作品,均为本网合法拥有版权或有权使用的作品,转载需联系授权。
2、凡本网注明“来源:XXX(非小桔灯网)”的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。其版权归原作者所有,如有侵权请联系删除。
3、所有再转载者需自行获得原作者授权并注明来源。
 /3
/3 