癌症是一种严重的疾病,对人类的健康和生命造成了巨大的威胁。大多数癌症死亡发生在肿瘤远处转移之后。转移的过程需要几年乃至几十年的时间,这为肿瘤发展到无法治愈阶段之前提供了足够的癌症早检窗口期。1
癌症早检对于提高癌症治愈率和生存率具有重要意义。在过去的十年里,基于液体活检的癌症早检引起了人们的极大兴趣,它能够识别各种生物分子特征,并有可能指示疾病的早期状态。
癌症早检作为一个新兴的商业模式,具有巨大的发展潜力和商业机会。目前,投资者和大公司越来越愿意投资基于液体活检的癌症早检领域。2,3 这种意愿的改变可能是“由于人们日益认识到癌症早检将改变癌症治疗”的商业模式。
癌症早检(Early Detection),是指通过一系列检查手段,对目标人群(包括无症状人群和有症状人群)进行癌症检测,以期早期发现肿瘤或癌前病变。癌症早检的目的是通过早期发现和治疗,降低癌症的发病率和死亡率,它包括癌症早筛(Early Screening,重点是尽早发现有疾病但无症状患者)和癌症早诊(Early Diagnosis,重点是尽早发现有症状患者)两种方式。4,5
癌症早检 = 癌症早筛(无症状)+癌症早诊(有症状)。
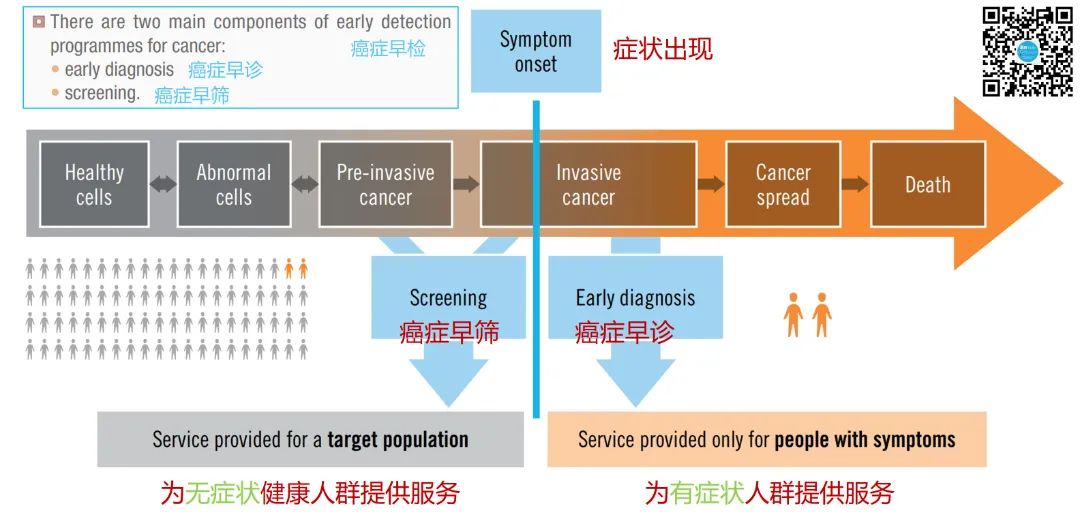
▲ 根据症状出现与否区分癌症早筛和癌症早诊
癌症早筛和癌症早诊是相互关联的,它们共同构成了癌症的早发现、早诊断和早治疗的过程。通过这些措施,可以有效地降低癌症的发病率和死亡率,提高治愈率和生存率。
据公开报道,迄今为止,基于液体活检的多癌早检(MCED)产品一直在努力的方向都是针对无症状健康人群。6 另外,从事实上来说,许多癌症在早期都是无症状的。7 因此,我们可以说:
癌症早检 ≈ 癌症早筛。
理想情况下,多癌早检/早筛产品应该具有非常高的特异性(低假阳性结果),以尽量减少不必要的检查和患者焦虑;同时,需保证在泛癌种范围内保持足够高的灵敏度(真阳性结果)。这确保了癌症早检/早筛产品能够检测出有临床意义的早期癌症,以降低相关癌症总死亡率。相关的前瞻性研究结果有:(1)DETECT-A研究中使用的CancerSEEK检测,PPV(阳性预测值)为28.3%,特异性为99.6%;(2)PATHFINDER研究中使用的GRAIL MCED检测,PPV为38%,特异性为99.1%。8,9
癌症不是一种疾病,而是多种多样的疾病,基本上可以起源于人体的所有细胞类型和器官,有一百多种不同的实体,具有不同的风险因素和流行病学特征。目前的传统筛查方式往往伴随着某些挑战。
液体活检有可能弥补这些不足,并补充筛查试验,以提供更有效的诊断平台。基于液体活检的癌症早筛策略包括检测和监测循环肿瘤DNA(ctDNA)、循环肿瘤细胞(CTCs)和细胞外囊泡(EVs)等。
(1)ctDNA:释放到生物体液中的DNA片段。它们是研究肿瘤特异性突变、CNV、甲基化变化或整合病毒序列的有力标志物。
(2)CTCs:原发性肿瘤释放到生物体液中的肿瘤细胞,并被认为具有转移潜能。
(3)EVs:肿瘤细胞释放出来的膜状结构,含有核酸(DNA、mRNA、miRNA、非编码RNA)、蛋白质、脂质或其他代谢物。
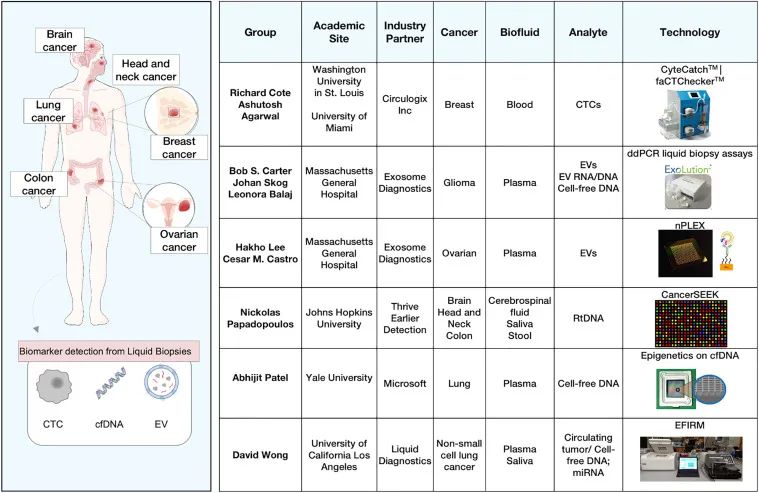
▲ 基于液体活检的癌症早筛技术研究
液体活检,是一个包罗万象的术语,主要是指对包括血液、尿液、脑脊液和唾液等在内的体液进行检测。美国国家癌症研究所(NCI)对液体活检的定义为:“对血液、尿液或其他体液样本进行的实验室检测,以寻找释放到体液中的CTC或ctDNA、ctRNA或其他分子片段。液体活检允许在一段时间内重复采样,可用于癌症早检,也可用于指导治疗方案制定或了解治疗效果如何,或癌症复发”。10
基于液体活检的癌症早检技术或方法:
(1)CTCs:循环肿瘤细胞
1869年,Ashworth首次描述了循环肿瘤细胞(CTCs)。CTC根据癌症类型有不同的分子标记,其中,由于大多数癌症都是上皮型的,所以有一种“通用的”上皮分子标志物 —— EPCAM —— 可以用来检测CTC,其表达随癌症类型不同而变化,主要应用在EPCAM表达强烈的乳腺癌、结直肠癌和前列腺癌等癌症上。
一般来说,CTC在血液中的浓度非常低,即使在转移性癌症患者中,每ml血液的CTC数量<10个。11 这也就意味着将CTC用作癌症早检的方法依然具有挑战性。
CellSearch系统是美国FDA批准的血液CTC检测产品,以鉴别、分离和计数上皮来源的CTC,用以评估转移性乳腺癌、结直肠癌和前列腺癌患者的预后。TAT为一周,费用为900美元。
(2)cfDNA/ctDNA:细胞游离DNA/循环肿瘤DNA
1948年,Mandel和Métais首次描述了cfDNA,它存在于健康人和患者体内。ctDNA是cfDNA的一部分,于1977年被发现。在癌症患者中,ctDNA占整体cfDNA的1%~2%,通过肿瘤特异性甲基化标记和体细胞突变等表观和遗传改变检测,可以区分正常cfDNA和ctDNA片段。
DNA甲基化是一种表观遗传机制,在人体内可自然发生,但经确认,异常的DNA甲基化模式可作为癌症早检的生物标志物(目前大多数cfDNA甲基化产品灵敏度相对较低,特异性更高)。在癌症早检方面,由最常见癌症特异性甲基化标志物组成的panel(多种甲基化标志物在多种癌症中很常见)将能够在肿瘤溯源方面获得更多的诊断信息,而且比单一检测标志物更有效。12
(3)EVs:细胞外囊泡
20世纪60年代末,Bonucci和Anderson首次报道在骨细胞中发现了小的分泌性细胞外囊泡。EVs有三种主要类型:外泌体、微泡(MVs)和凋亡小体,它们根据其大小、内容物、功能、释放途径和生物发生而有所区别。EVs所携带的分子信息被认为是原细胞的分子指纹,因此被认为是潜在的癌症生物标志物。
EVs比ctDNA和CTCs更有优势,它们具有双层膜结果,不易降解,并且可以很好的保护原始细胞的生物信息来源。基于EVs蛋白谱的血液检测产品已被用于I期和II期胰腺癌、卵巢癌和膀胱癌的检测。13
(4)Proteins:蛋白质
基于蛋白质生物标志物检测的液体活检在癌症早检和疾病监测方面具有巨大潜力,比如PSA,CA-125等。临床研究显示,为提高诊断准确性,并减少假阳性和假阴性,应使用多个蛋白质的panel或蛋白质和DNA生物标志物的组合。14
(5)cfRNA:细胞游离RNA
cfRNA是由坏死细胞或凋亡细胞降解并释放到血液中的RNA片段。ctRNA是cfRNA的一部分,与ctDNA相比,ctRNA被认为是一种不稳定的分子,在血浆中的“裸”半衰期大约只有15秒,远低于ctDNA的1分钟~2.5小时。这种不稳定性限制了ctRNA的临床应用,并且还没有确定最佳的提取方法。
当前,围绕血液中的mRNA、ncRNA和miRNA等研究较多。其中miRNA是最受关注的一类,这主要归咎于其稳定性,以及在大多数人类癌症中,miRNA水平会发生变化且其表达具有组织特异性。既往一项荟萃分析研究,全面评估了miRNA在血液肿瘤诊断中的总体准确性,总体特异性为85%,灵敏度为81%,表明miRNAs可以区分健康个体和血液肿瘤患者。15
(6)TEP:肿瘤诱导血小板
血小板是由巨核细胞产生的无核小圆盘状细胞片段,存在于血液和脾脏中。血小板本身无法合成RNA,而是从循环中内吞或从巨核细胞中获得RNA。当血液流经肿瘤时,血小板会与肿瘤细胞发生相互作用。此时,一些血小板受到“肿瘤教育”而表现出改变的RNA谱和蛋白质谱。这种变化可以作为生物标志物,并用于区分健康个体和泛肿瘤患者。16
(7)自身抗体
自身抗体是抗体的一种形式,它与人体自身形成的物质发生反应(如自身抗原)。这些自身抗原可能只存在于身体某一器官的特定细胞类型中,也可能存在于所有细胞类型中,它们可以在自身免疫性疾病和癌症中发现,并被证明是有用的疾病生物标志物。
自身抗体检测在肺癌早检中已经显示出成功。Sullivan等人研究了多组学液体活检公司Oncimmune的EarlyCDT-Lung产品(美国Biodesix)在检测血清肿瘤相关抗原自身抗体方面的潜力。除了Oncimmune公司以其液体活检技术引领自身抗体检测市场以外,其他公司也提供自身抗体检测,如GeneCopoeia™及其OmicsArray™抗原微阵列。17
(8)光谱检测
另一种液体活检策略是采用振动光谱法,特别是衰减全反射(ATR)傅里叶变换红外光谱(FTIR),再加上机器学习。数十年来,红外光谱分析生物标本作为癌症诊断工具的潜力一直是众所周知的。生物标本,如胆汁,血液,细胞外囊泡和尿液已经研究使用FTIR光谱,以帮助找到替代癌症诊断方法,以及癌症管理技术。FTIR是一种简单、无标签、快速、廉价、无创、无损的分析方法。18
综合来看,液体活检是癌症早检的未来。但当前市场基于液体活检的癌症早检产品主要是基于基因组学层面,即cf/ctDNA,且目前大多数液体活检技术缺乏早期癌症的检测能力。因此,通过多种技术的结合,有望实现对多种癌症的有效检测。
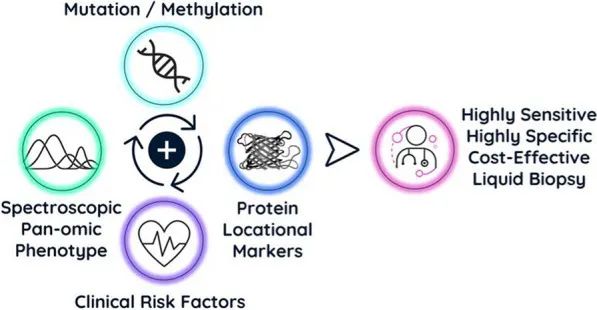
▲ 多种技术结合,有望实现多癌早检
上半文,
至此告一段落,
如果你有时间,可接着阅读“癌症早检的挑战”:
尽管最新的研究显示,癌症早检可以挽救患者生命,但仍需要进一步创新和开发癌症早检方法。由于生物学认识的进步和技术发展速度的加快,该领域正在迅速发展,但也同样面临诸多挑战。
2022年3月18日,《Science》(IF:56.9)发表了癌症早检的文章,提出了当前癌症早检的五大挑战。19
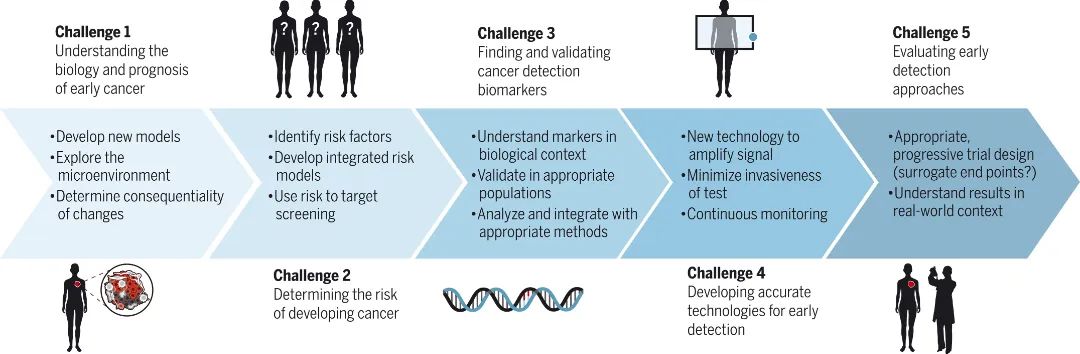
▲ 癌症早检的五大挑战
挑战一)建立对早期癌症生物学特性的理解。
肿瘤发生是一个从正常到失调再到癌变的连续过程。一个关键的挑战是理解这种生物学特性,以便我们能够预测我们所检测到变化的未来轨迹,并有助于区分严重的、侵袭性的病变和不造成伤害的病变,将过度诊疗的风险降至最低。
挑战二)确定罹患癌症的风险。
了解谁、如何和何时进行检测,以及如何解释检测结果,需要了解个体患癌风险。癌症早检策略对每个人的价值并不相等。因此,重要的是查明癌症风险较高的人群(如何利用胚系基因组易感性、家族史、暴露史、人口及年龄统计和行为数据来构建精细的风险模型),并针对这一群体制定癌症早检策略,以最大限度地发挥癌症早检的益处,并最小化过度诊断和不充分诊断及治疗带来的危害。
挑战三)寻找并验证癌症早检的生物标记物。
一个关键的挑战是如何在正常人类生物学的噪音中检测早期癌症的微小信号。虽然历史上进展缓慢,但许多有前景的早期检测标志物正在出现,包括ctDNA,CTC,蛋白质、外泌体和癌症代谢物。
诊断检测的两个基本指标是灵敏度和特异性。灵敏度是指检测正确识别阳性患者的能力(真阳性率),灵敏度较高的检测不会漏诊(即,不会出现假阴性)。特异性是指正确识别阴性患者的能力(真阴性率),特异性高的检测不会在阴性的情况下给出阳性的结果(即,不会出现假阳性)。灵敏度和特异性既取决于检测中使用的技术,也取决于所检测的生物标志物。
另外两个关键指标是阳性预测值(PPV,即检测呈阳性的人实际上罹患癌症的概率)和阴性预测值(NPV,即检测呈阴性的人实际上未患癌症的概率)。这些参数的目标值将取决于使用检测的预定情况和特定癌症在特定人群中的流行程度。
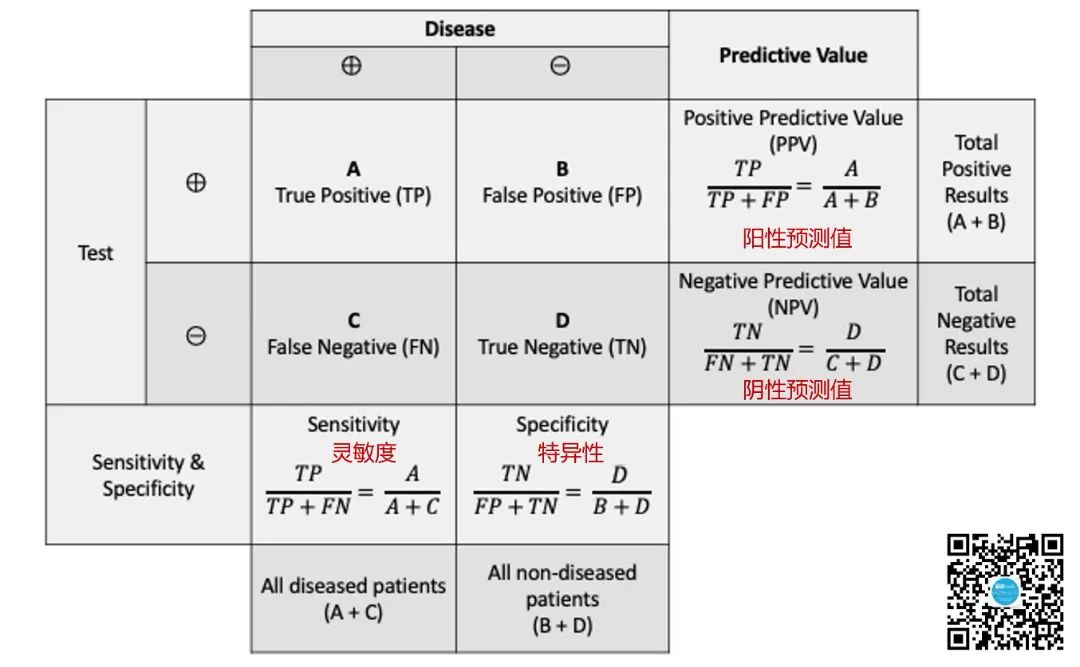
▲ 灵敏度/特异性/PPV和NPV
挑战四)开发并用于癌症早检的精确技术。
开发具有检测早期肿瘤的灵敏度和最小化假阳性的特异性技术是一个关键的挑战。新技术的出现使早期癌症检测的准确性不断提高。癌症早检的目标之一是检测容易治疗且不太可能转移的实体肿瘤。这通常意味着在支持增强血管生成和抑制抗肿瘤免疫的肿瘤微环境形成之前,此时肿瘤直径约为1mm(由105~106个细胞组成)。大多数临床使用或正在开发的影像技术无法检测到如此微小的肿瘤,强大的液体活检分子分析技术、先进的影像(MRI等)、组织病理学和AI方法正在提高发现早期肿瘤的能力,而使用合成标记物可能有助于放大其信号。
挑战五)如何适当地评价癌症早检方法。
癌症早检方法和试验设计存在诸多挑战。试验必须仔细设计,以解决相关人群的问题并测量适当的终点,并为临床实践提供有力的统计学证据。癌症早检试验与药物治疗临床试验不同,癌症早检需要专业的统计学知识以指导研究设计和适当的样本规模大小。例如,癌症早检试验的统计功效受多种因素影响,而药物治疗试验则不会受这些因素影响,比如一个人接受检测的次数、检测之间的时间间隔以及进行检测的年龄等。癌症早检试验中要考虑的终点与药物治疗试验中的终点不同,监管审批途径也不同。最后,癌症早检试验的主要挑战还是在于其规模和解读。
2023年10月17日,《Cell Reports Medicine》(IF:14.3)发表了癌症早检的挑战和机遇,探讨了基于当前液体活检技术方法在癌症诊断和监测中的作用和挑战。20

▲ 液体活检联盟:癌症早检与监测的挑战和机遇
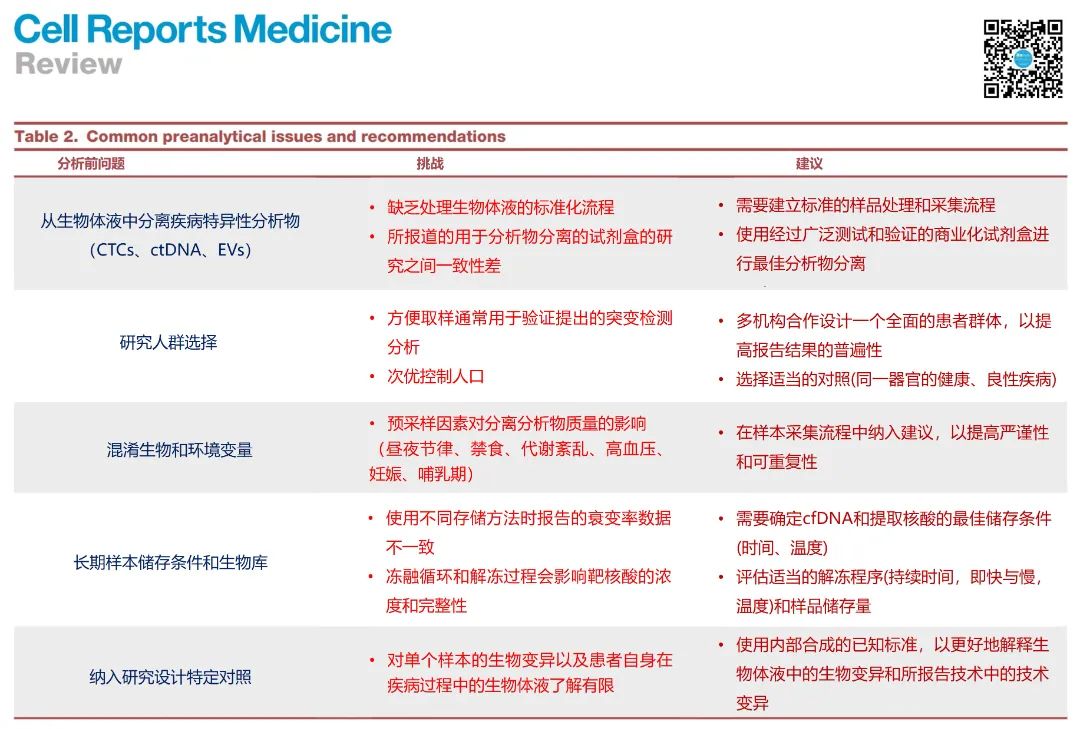
▲ 常见分析前问题、挑战和建议
总的来说,基于液体活检的癌症早检在面临挑战的同时,也带来了许多机遇,有望在未来成为早期癌症检测的重要工具。
参考资料:
1.Vogelstein B, Papadopoulos N, Velculescu VE, Zhou S, Diaz LA Jr, Kinzler KW. Cancer genome landscapes. Science. 2013 Mar 29;339(6127):1546-58.2.D. Schenkel, S. Nambi, R. Blicker, C. Lin, Liquid Biopsy: Early Detection of a Huge Investment Opportunity.3.Grand View Research, “Cancer diagnostics market worth $249.6 billion by 2026,” February 2019.4.Guide to cancer early diagnosis.WHO 20175.Early Detection.(Cancer control : knowledge into action : WHO guide for effective programmes ; module 3.).WHO 20076.Wang Y, Tie J. Blood Test for Multicancer Detection in Symptomatic Individuals. JCO Precis Oncol. 2023 Sep;7:e2300305.7.Siegel RL, Miller KD, Fuchs HE, Jemal A. Cancer statistics, 2022. CA A Cancer J Clinicians. 2022;72(1):7–33.8.Lennon AM, et al. Feasibility of blood testing combined with PET-CT to screen for cancer and guide intervention. Science. 2020 Jul 3;369(6499):eabb9601.9.Schrag D, McDonnell CH III, Nadauld L, et al: A prospective study of a multi-cancer early detection blood test. Ann Oncol 33:S417-S426, 202210.https://www.cancer.gov/publications/dictionaries/cancer-terms/def/liquid-biopsy11.Wu TM, Liu JB, Liu Y, Shi Y, Li W, Wang GR, et al. Power and promise of next-generation sequencing in liquid biopsies and cancer control. Cancer Control. 2020;27(3):107327482093480.12.Laird PW. The power and the promise of DNA methylation markers. Nat Rev Cancer. 2003;3(4):253–266.13.Hinestrosa JP, Kurzrock R, Lewis JM, Schork NJ, Schroeder G, Kamat AM, et al. Early-stage multi-cancer detection using an extracellular vesicle protein-based blood test. Commun Med. 2022;2(1):29.14.Landegren U, Hammond M. Cancer diagnostics based on plasma protein biomarkers: hard times but great expectations. Mol Oncol. 2021;15(6):1715–1726.15.Drokow EK, Sun K, Ahmed HAW, Akpabla GS, Song J, Shi M. Circulating microRNA as diagnostic biomarkers for haematological cancers: a systematic review and meta-analysis. CMAR. 2019;11:4313–4326.16.Best MG, Sol N, Kooi I, Tannous J, Westerman BA, Rustenburg F, et al. RNA-Seq of tumor-educated platelets enables blood-based pan-cancer, multiclass, and molecular pathway cancer diagnostics. Cancer Cell. 2015;28(5):666–676.17.https://www.genecopoeia.com/product/cancer-and-neoplasms-antigen-microarray/18.Butler HJ, Brennan PM, Cameron JM, Finlayson D, Hegarty MG, Jenkinson MD, et al. Development of high-throughput ATR-FTIR technology for rapid triage of brain cancer. Nat Commun. 2019;10(1):4501.19.Crosby D, Bhatia S, Brindle KM, Coussens LM, Dive C, Emberton M, Esener S, Fitzgerald RC, Gambhir SS, Kuhn P, Rebbeck TR, Balasubramanian S. Early detection of cancer. Science. 2022 Mar 18;375(6586):eaay9040.20.Batool SM, et al. The Liquid Biopsy Consortium: Challenges and opportunities for early cancer detection and monitoring. Cell Rep Med. 2023 Oct 17;4(10):101198.
 /3
/3 