NMPA已经批准的癌症甲基化“早筛”试剂盒汇总如下:

现在虽然已经有不少癌症“早筛”甲基化试剂盒获批,但主要集中在肠癌上。SDC2基因是基于粪便样本的肠癌甲基化试剂盒的“明星靶点”,Septin9基因是基于血液样本的肠癌甲基化试剂盒的“明星靶点”。 应该选择哪个肠癌甲基化试剂盒? 粪便 VS 血液,孰优孰劣? 基于NMPA公开的审评报告数据,两者性能在伯仲之间,但是基于粪便的样本验证数据更多,应更加可靠一些。
样本类型相同时,基因靶点数目越多,性能理论上越好;
粪便样本可以居家取样,但血液样本的接受率和肠镜依从率更高。
两者都不可替代肠镜!!! 肠镜依然是金标准。鉴于国内肠镜价格不贵,你如果是肠癌高风险人群,又不怕肠镜的麻烦过程,建议直接做肠镜。
其它癌症的性能表现如何,还是以NMPA医疗器械技术审评中心发布的技术审评报告为准,上表众多试剂盒中,只有以下几个(下表)公开了对应的技术审评报告,一个癌种正好一个:
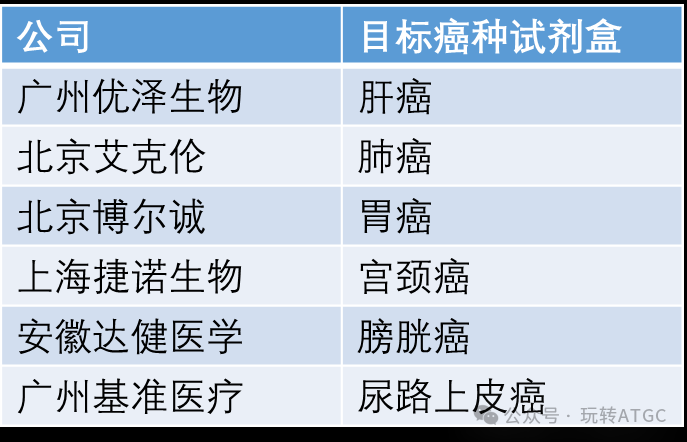
下面依次进行解读: 广州优泽生物-肝癌试剂盒 检测样本类型: 血液 检测靶点: BMPR1A/PLAC8 产品模型: 此产品是基于数字PCR平台,可以直接得到目标靶点的甲基化比例,阈值设置:BMPR1A基因≥5.5%或当4.0%≤BMPR1A基因<5.5%,PLAC基因≥10%为阳性;BMPR1A基因<4%或当4.0%≤BMPR1A 基因<5.5%,PLAC 基因<10%为阴性。 产品适用: 本产品适用于临床上对疑似原发性肝细胞癌、混合型癌的辅助诊断,包括临床肝区影像学检查和既有临床检查怀疑肝区占位性病变的患者,检测结果阳性不作为肝癌临床确诊的唯一依据,检测结果阴性也不能排除肝癌的可能。该检测不能作为肝癌早期诊断或确诊的依据,不宜用于普通人群的肿瘤筛查。训练集样本: 入组(包含建立和验证)样本数共计 1998例,包括肝细胞癌、肝细胞癌-肝内胆管癌(混合型癌)、良性肝脏疾病、其他肿瘤样本等。测试集样本: 纳入临床病例 1503 例,其中,非侵入性方法无法进行明确诊断的肝脏疾病病例 96 例,其
中肝癌病例 542 例,非肝癌的其他病例 979 例(包括其他易产生干扰的肿瘤及各种良性疾病病例)。性能表现: 北京艾克伦-肺癌试剂盒 检测样本类型: 血液 检测靶点: SHOX2/RASSF1A/PTGER4 产品模型: 逻辑回归 产品适用: 本产品用于临床上对疑似肺癌患者的辅助诊断,检测结果阳性不作为肺癌早期诊断或确诊的证据,检测结果阴性也不能排除肺癌的可能。 该检测不能作为肿瘤早期诊断或确诊的依据,
不宜用于普通人群的肿瘤筛查。 训练集样本: 有效样本数共计489 例,包括肺部正常样本 207 例、肺癌病人样本 141 例、其它干扰样本(包括结节、肺炎、肺结核、囊肿、食管癌、胃癌等)141 例。测试集样本: 有效例数 248 例,包括肺部正常人样本 81例,肺癌病人样本 76 例,其他干扰样本 91 例。性能表现: 特异性为 94.19%,灵敏度为 89.47%,总符合率为 92.74%。 北京博尔诚-胃癌试剂盒 检测样本类型: 血液 检测靶点: RNF180/Septin9 产品模型: 单靶点判别模型,当RNF180基因、Septin9基因分别有一个为检测阳性或两个均为检测阳性时,可判定为检测阳性。 产品适用: 该产品适用于经临床医师诊断建议胃镜检查同时由于患者个人原因拒绝进行胃镜检查的患者。检测结果阳性不作为胃癌早期诊断或确诊的证据,检测结果阴性也不能排除胃癌的可能,患者最终诊断应依据胃镜检查结果。该产品不用于普通人群的肿瘤筛查。基于现有研究,仅限于有胃癌家族史者或40 岁以上胃癌高风险人群检测。 训练集样本: 对 961 例临床样本进行检测,其中包括其中胃癌样本 393 例( I 期 66 例、II 期 68 例、III 期 173 例、IV 期 33 例、分期不明 53 例),浅表性胃炎样本 184 例,萎缩性胃炎样本 170 例,其他胃部疾病样本 39 例,其他癌症样本 175 例(大肠癌、食管癌、胰腺癌等)。 测试集样本: 共筛选有效病例 1382 例。其中胃癌病例 680 例,非胃癌病例 702 例。胃癌病例涵盖了胃癌不同分期的患者,占总入组病例数的 49.20%( 680/1382)。非胃癌病例包括交叉反应人群样本共 702 例,其中含对照组共 536例( 包括:浅表性胃炎、萎缩性胃炎、胃息肉、 肠化生、 低级别内瘤变、 其它胃良性疾病及其它疾病(胃溃疡、糜烂性胃炎等) 和良性肿瘤), 166 例其它癌症样本( 包括主要高发癌症:肺癌、肝癌、乳腺癌、食管癌和肠癌;还有发病率较低的癌症:胰腺癌和卵巢癌)。 检测灵敏性为 61.76%( 420/680),特异性为 85.07%( 456/536)。试剂盒检出 I 期灵敏性为 50.00%,Ⅱ 期的灵敏性为 62.32%, Ⅲ期的灵敏性为 67.68%, Ⅳ期的灵敏性为 82.00%,分期不明灵敏性为 55.88%。上海捷诺生物-宫颈癌试剂盒 检测样本类型: 宫颈脱落细胞 检测靶点: ASTN1、 DLX1、ITGA4、 RXFP3、 SOX17、 ZNF671 产品模型: 采用逻辑回归分析方法确定模型中 6 个基因的权重, 建立 6 个基因的评分, 然后根据约登指数最大的原则确定最佳阈值。产品适用: 本产品适用于 12 种高危 HPV( hrHPV)基因型( 31、 33、 35、39、 45、 51、 52、 56、 58、 59、 66、 68 型)检测阳性的 30 岁以上女性人群,帮助识别是否需要进行阴道镜检查,达到分流管理的目的。使用本产品检测,当检测结果为阴性时,提示无宫颈病变或宫颈病变级别较低的可能性较大,可避免阴道镜及组织活检检查,做好定期复查;检测结果为阳性时,提示宫颈病变级别较高的可能性大,需进一步进行阴道镜和/或组织活检检查。 训练集样本: 636 例样本中≤ CIN1(轻度不典型增生) 病例 503 例, CIN2 (中度不典型增生)病例 85 例,≥ CIN3 (重度不典型增生和原位癌)病例48 例。 测试集样本: 临床试验前瞻性入组 12 种 hrHPV 检测阳性病例 1112 例, 30 岁以上适用人群受试者 746 例, 其中阴道镜和/或组织病理学检查为阴性的病例473 例, CIN1 病例 157 例, CIN2 病例 73 例,≥ CIN3 病例 43 例。 性能表现: 针对 30 岁以上 12 种 hrHPV 检测阳性的人群: 以 CIN2 为临床诊断界值, 试验体外诊断试剂临床灵敏度为 86.21%,特异度为 93.97%,阳性预测值为 72.46%,阴性预测值为 97.37%。以 CIN3 为临床诊断界值, 试验体外诊断试剂临床灵敏度为95.35%,特异度为 86.20%,阳性预测值为 29.71%,阴性预测值为 99.67%。试验结果显示,试验体外诊断试剂用于 12 种 hrHPV 检测阳性患者分流时,与宫颈细胞学检查相比,在灵敏度基本一致的情况下,特异度显著提高( P< 0.0001),可有效降低不必要的阴道镜转诊数量。 安徽达健医学-膀胱癌试剂盒 检测样本类型: 尿液 检测靶点: Twist1 产品模型: 单靶点诊断模型,采用 ROC 曲线法和约登指数确定试剂盒阳性判断值为 10。当Δ Ct 值≤ 10 时判断为阳性,Δ Ct 值> 10 时,判断为阴性。 产品适用: 本试剂盒适用于血尿、尿频、尿急和尿痛等临床上疑似膀胱癌、临床诊断建议进行膀胱镜检查患者的辅助诊断。本产品仅作为现有诊断方法的补充和辅助,供临床医师参考。训练集样本: 有效样本数共计 164 例,样本来源包括膀胱癌患者、肾细胞癌患者、前列腺癌患者、输尿管癌患者、肾盂癌患者、输尿管炎、尿路上皮增生、膀胱无病变人群等。测试集样本: 纳入临床有效病例 1233 例,其中膀胱癌病例 348 例(覆盖膀胱癌所有分期及病理分型),非膀胱癌的其它病例 885 例(包括其它易产生干扰的肿瘤及各种良性疾病病例)。性能表现: 本产品临床灵敏度为 88.2%,特异度为 86. 8%,总符合率为 87.2%。广州基准医疗-尿路上皮癌试剂盒 检测样本类型: 血液 检测靶点: ONECUT2/VIM 产品模型: 单靶点判断模型,其中VIM 基因 Ct 阈值为 38.6, ONECUT2 基因 ΔCt 阈值为 5.7。产品适用: 适用于有血尿、膀胱刺激症等临床症状,或经影像学等非侵入性方法显示异常,临床可能需进一步检查的疑似尿路上皮癌初诊患者的辅助诊断,尤其是经影像学等非侵入性方法无法决策病例是否进行膀胱镜检查的辅助诊断。可为患者提供一种尿路上皮癌的无创辅助诊断选择,但不能作为肿瘤早期诊断或确诊的依据。临床医生应结合患者病情及其它实验室检测指标等因素对检测结果进行综合判断。 训练集样本: 纳入的阳性病例286 例,包括膀胱癌、肾盂癌、输尿管癌三种尿路上皮癌初诊患者;阴性病例共纳入 386 例,包括泌尿系统良性疾病和泌尿系统其它恶性肿瘤以及非泌尿系统恶性肿瘤,共计 672 例。 测试集样本: 共纳入临床有效病例 1172 例,其中尿路上皮癌病例 429 例(覆盖尿路上皮癌所有分期及病理分型),非尿路上皮癌的其它病例 743 例(包括其它易产生干扰的肿瘤及各种良性疾病病例)。 性能表现: 本产品临床灵敏度为 89.74%,特异度为 92.46%,总符合率为 91.47%。
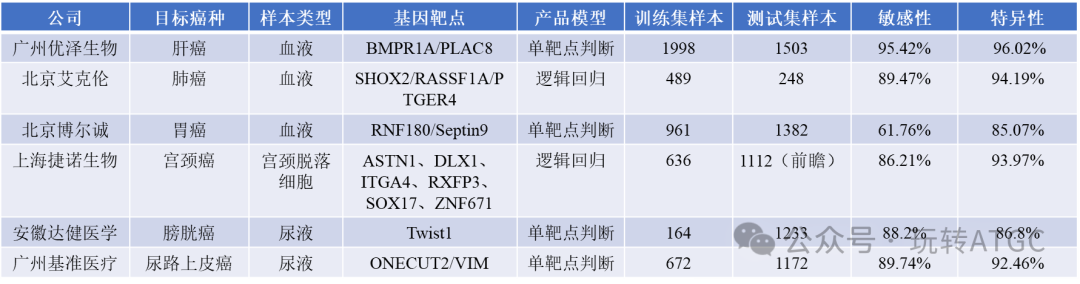
总结几点如下: 需要的临床样本数目,除了北京艾克伦的肺癌试剂盒,其它都在1000+。
除了广州优泽生物使用数字PCR平台,其它都使用荧光定量PCR平台,数字PCR平台可以直接测得目标靶点的甲基化比例,分辨率更高。
上海捷诺生物的宫颈癌试剂盒,也是前瞻性收集的样本,是除了诺辉健康常卫清之外的第二个前瞻性验证。
注册收集样本时,除了收集目标癌种的样本,为何还要收集其它癌种的众多样本?
因为很多甲基化标志物在可能在多个不同的癌种中都有癌症信号,只是信号强度有所差异,就需要尽量筛选癌种特异性的甲基化标志物,需要保证试剂盒对目标癌种的敏感性远高于其它癌种。
现所获批试剂盒适用的样本类型包括粪便,尿液,宫颈脱落细胞,血液。但是粪便样本只适用于肠癌,尿液只适用于膀胱癌/尿路上皮癌,宫颈脱落细胞只适用于宫颈癌,只有血液适用癌种最广,现在已覆盖了肠癌,肝癌,肺癌和胃癌。
鉴于现在基于血液cfDNA甲基化靶向测序的泛癌早筛产品已经证实了甲基化在众多癌症中的性能(参考Grail的一堆结果及国内相关进展-国内泛癌早筛产品梳理之甲基化靶向测序篇),下一个基于血液的单癌种甲基化试剂盒会是哪一个癌种呢?
参考资料(审评报告链接): 北京博尔诚-胃癌: https://www.cmde.org.cn//xwdt/shpbg/20200508141000124.html 安徽达健医学-膀胱癌: https://www.cmde.org.cn//xwdt/shpbg/20221117091541126.html 广州优泽生物-肝癌: https://www.cmde.org.cn//xwdt/shpbg/20230627090655107.html 上海捷诺生物-宫颈癌: https://www.cmde.org.cn//xwdt/shpbg/20220901110621132.html 北京艾克伦-肺癌: https://www.cmde.org.cn//xwdt/shpbg/20220223140900607.html 广州基准-尿路上皮癌: https://www.cmde.org.cn//xwdt/shpbg/20240219085318114.html
|  /3
/3 