严重先天性心脏缺陷胎儿的遗传诊断率
2021-4-13 14:31|
编辑: 沙糖桔|
查看: 3313|
评论: 0|来源: 基因检测与解读 | 作者:陈美华
摘要: 背景介绍先天性心脏缺陷(CHDs)是最常见的先天性出生缺陷,患病率为5-8/1,000个活产儿。大约三分之一的病例涉及严重的CHDs。尽管在过去几十年中,CHD患儿的生存率有了显著提高,但其发病率依旧相当高(与疾病相关) ...

先天性心脏缺陷(CHDs)是最常见的先天性出生缺陷,患病率为5-8/1,000个活产儿。大约三分之一的病例涉及严重的CHDs。尽管在过去几十年中,CHD患儿的生存率有了显著提高,但其发病率依旧相当高(与疾病相关),预期寿命也仍然是降低的。众所周知,非整倍体(染色体数目异常),如13、18、21三体和Turner综合征均与CHDs有关。亚显微缺失或重复(通常被称为拷贝数变异(CNVs)),在约10%-15% 的CHD儿童中有报道。由于这些CNVs对CHD儿童的发育、生活质量和预期寿命有重大影响,因此在大多数发达国家,染色体微阵列分析(CMA)是胎儿护理的标准。然而,在CHD病例中,出生后或儿童期才诊断出遗传综合征的情况并不少见,因为某些序列变异是CMA无法检测到的。虽然CHDs已被描述为许多遗传综合征的一部分,但只有少数队列研究报告了诊断为CHD的胎儿的遗传诊断(染色体异常或序列变异)。之前一些在胎儿队列中进行的研究已经过时了,因为它们主要集中在非整倍体异常。这限制了产前咨询,因为目前可用的数据大多基于出生后的研究。出生后队列中的遗传诊断率预计是偏低的,因为终止妊娠(TOP)、胎死宫内或新生儿早期死亡的病例往往不包括在这些队列中。另一点更为重要的是,由于胎儿的临床表型会不断演变,大多需要出生后进行测序,这使得在妊娠中期评估遗传综合征的产前患病率变得困难。在产前,对可能被认为是CHD遗传原因或次要发现的遗传变异比率的了解,可以改善严重CHD病例的产前咨询。这些基因诊断的准确数据将有助于专业人员决定是否使用目前可用的其他检测,如外显子组测序(ES)或特定遗传综合征的基因检测。本研究旨在通过评估产前和产后基因检测的结果,对患有严重CHDs的胎儿中染色体异常和序列变异的比例进行保守估计,特别是在排除非整倍体之后。ES在CHDs胎儿中的潜在诊断率,以及一些可能增加遗传诊断机会的因素,也将进行评估。从PRECOR注册表中提取了2012年1月至2016年12月期间诊断为严重CHD患者,共919例。父母选择侵入性产前检测的有542例(59.0%),而出生后进行基因检测的有185例(20.1%)。所有这些病例都进行了非整倍体检测。919例中有192例(20.9%)未在产前或产后进行基因检测。在这些病例中,父母要么拒绝基因检测,要么没有提示基因检测,由于缺乏畸形特征,CHD不被认为与遗传综合征有关。经过遗传学家的临床评估,大多数病例(173/192,90.1%)出生后没有遗传综合征的迹象,而9.9%(19/192)的病例确实有心外畸形(ECMs)(图1)。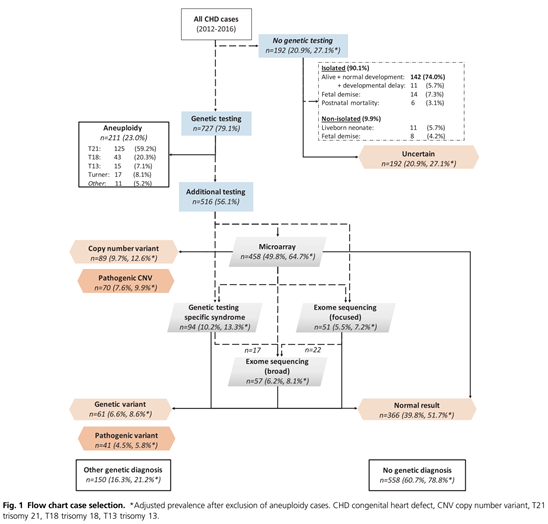
在919例CHD患者中,有211例(23.0%)为非整倍体异常。由于我们关注的主要是染色体结构异常和序列变异的比例,而不是非整倍体异常。因此,只有708个病例被纳入到进一步的分析中。这些病例中的基因检测涉及CMA的占64.7%(458/708),特定综合征的基因检测占13.3%(94/708),目标区域外显子组测序分析占7.2%(51/708)或全外显子组测序分析占8.1%(57/708)。这些病例的基线特征作为补充材料附在表S1中。通过将妊娠期报告的所有遗传变异(包括“意义未明的”)与出生后检测到的遗传变异进行整合,确定该队列中患有CHD的胎儿中有染色体异常和序列变异的比例。将该队列中检测到的所有遗传变异总结概括在表1中。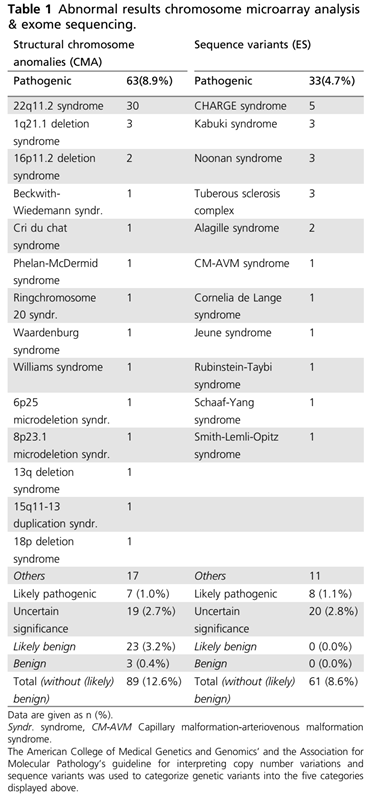
在708例无非整倍体异常的重度CHD患者中,有111例(15.6%)得到了基因诊断。其中70例(9.9%)通过CMA诊断为拷贝数变异(CNVs),这70例CNVs异常胎儿中, 63例为致病性CNVs,7例为可能致病性CNVs。在2.7%(19/708)的病例中发现意义未明的CNVs。22q11.2缺失综合征是最常见的微缺失综合征,占比为4.2%(30/708),占所有(可能)致病性CNVs的42.9%(30/70)。在41例(41/708,5.8%)患有CHD的胎儿中,通过额外的检测发现了潜在的可能导至CHD的序列变异。其中33例为致病性变异,8例为可能致病性变异。在2.8%(20/708)的病例中发现了意义未明的序列变异。常见的遗传综合征包括CHARGE综合征(5/41,12.2%)、Kabuki综合征(3/41,7.3%)和Noonan综合征(3/41,7.3%)。在65.9%(27/41)的(可能的)致病性序列变异中,基于临床指征进行了特定综合征(例如Kabuki综合征或Noonan综合征)的基因检测。在大多数病例中(16/27,59.3%),这些变异是在出生后确诊的。其余34.1%(14/41)的(可能的)致病序列变异是通过靶基因外显子组测序分析或全外显子组分析检测到的。为了比较靶基因panel分析与全外显子组分析这两种ES数据分析策略的优势和局限性,我们分析了与所有报道的序列变异(包括“意义未明的”)相关的诊断率。在所有检测到的序列变异中,有24.6%(15/61)的变异为与CHDs无关基因的(可能的)致病性变异。因此,如果仅使用靶向CHD基因组分析ES数据,则一些显著的变异,例如引起毛细血管畸形-动静脉畸形综合征的RASA1序列变异或导至结节性硬化的TSC1基因中的变异(产前未怀疑)将不能被检测到。而全外显子组分析的缺点是增加了对“意义未明的”的变异的鉴定,这类变异占所有鉴定的序列变异的19.7%(12/61)。85% (94/111)的染色体结构异常和序列变异被认为是心脏缺陷发生的确切原因,这意味着在13%(94/708)的整倍体CHD病例中,发现了心脏缺陷的遗传原因。在接受基因检测的患者中,这一比例为18%(94/516)。次要发现包括遗传变异导至的严重血友病、腓骨肌萎缩症和精神运动发育迟缓。在随后的分析中,被分类为致病或可能致病的染色体结构异常和序列变异均被认为是致病性诊断,因此一并报道。其余无基因检测结果的病例被视为检测结果正常,而具有意义未明的变异的病例被单独报告。最常见的伴有遗传诊断的心脏缺陷包括主动脉弓断离(IAoA)、肺动脉闭锁伴室间隔缺损(PA-VSD)、(非)平衡性房室间隔缺损(AVSD)、动脉干和法洛四联症。而在室间隔完整的大动脉转位(单纯性TGA)、三尖瓣闭锁、左心室双入口或完全型肺静脉异位连接的胎儿中,遗传诊断率很低。在两个单纯性TGA病例中得到的遗传诊断都是不能解释心脏缺陷的次要发现。其中一例诊断为A型血友病,母亲是个携带者;而另一例为16q11.2缺失,是新发变异,与心脏缺陷相关性不大。对于每个常见的CHD和单独的病例,遗传诊断率如表2所示。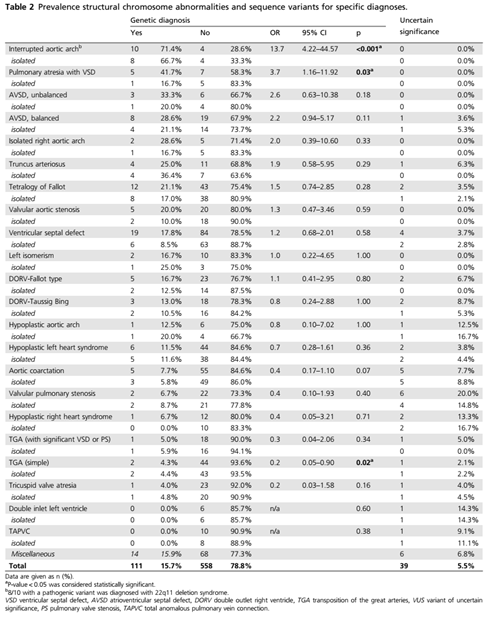
产前孤立性CHD病例的基因诊断率(11.6%,63/541)明显低于非孤立病例(28.7%,48/167)(p<0.001)。自述的血缘关系(35.5%vs 2.9%,p=0.002)和父母有冠心病病史(32.3%vs 3.8%,p=0.03)也与遗传诊断显著相关。其他相关变量,如母亲年龄、妊娠、肥胖或多胎妊娠与基因诊断无显著相关性(表3)。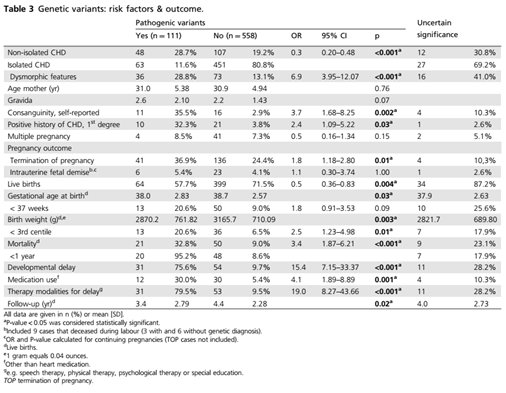
基因诊断对所有纳入病例妊娠结局的影响如表3所示。比较了有和没有基因诊断的病例的产后结果。首先,与没有获得基因诊断的父母相比,当胎儿心脏缺陷伴有基因诊断时,父母选择TOP的比例明显更高(36.9% vs24.4%;p=0.01)。检测到“意义未明的”的变异并不会导至TOPs的增加,因为得到意义未明变异检测结果的父母选择终止妊娠的比例甚至比那些基因检测结果正常的父母还更低(10.3%vs 24.4%;p =0.04)。这表明,与检测到“意义未明的”变异的结果相比,特异性诊断结果更能影响父母对TOP的决定。在有基因诊断的CHD病例中,出生体重<第三个百分点的病例比例较高(20.6% vs 6.5%;p =0.01)。有基因诊断的病例其出生后死亡率也增加(32.8% vs 9.0%,p < 0.001)。与没有遗传诊断的儿童(9.7%)相比,有遗传诊断的儿童(75.6%)更容易出现发育迟缓的体征(p < 0.001)。有基因诊断的病例往往不是因为心脏缺陷本身,而是因为其他原因需要药物治疗以及(医疗)支持(30.0% vs 5.4%,p =0.001),如语言治疗、物理治疗或特殊教育(79.5% vs 9.5%,p < 0.001)。在所有CHD胎儿中,(可能的)致病性CNVs的最低比例为7.6%(70/919)。对于不能用标准微阵列检测的序列变异,(可能的)致病性变异的比例估计为所有CHD胎儿的4.5%(41/919)(图1)。在所有CHD病例中,33% (305/919)找到了CHD的遗传原因,对于接受基因检测的患者,这一比例为42% (305/708)(补充材料,图S1)。本研究表明,即便在CMA阴性且接受靶基因检测情况下,仍有36.6%(15/41)的(可能的)致病变异将被遗漏。这种方法在产前环境中不太可取,由于胎儿的基本临床症状可能无法检测到,这可能导至对“错误的”基因panel进行分析。对全外显子组测序数据进行分析可以检测到整个外显子组的变化,但以周转时间或成本为代价。与CHDs无关的基因中的序列变异也可能增加额外发病率的风险。这可能对产前咨询很重要,因为它可以显著影响预后和新生儿管理。全外显子组范围的序列数据分析对于鉴定新的致病基因和改善目前可用的CHDs基因panels也非常必要。结果表明,在所有检测到的序列变异中,意义未明的变异占19.7%(12/61),这可能会使产前咨询和父母的决策复杂化。然而,我们相信,对CHDs胎儿的外显子组测序数据进行全外显子组分析的优势可能超过其造成的困难,特别是在合并其他结构畸形的情况下。这项研究的一个局限性是本队列中有20.9%的病例没有进行基因检测。然而,这些病例大多数是出生后没有畸形特征、发育正常的孤立病例。由于旅行距离相对较短,出生后进行基因检测的门槛非常低,所有儿童都在我们的中心进行了随访。因此,我们选择不排除病例,以避免重大的选择偏差,因为这可能导至对患病率的过高估计。。总之,本队列研究表明,在排除非整倍体异常后,在相当大比例的严重CHDs病例中可以发现染色体结构异常和序列变异。如果只进行CMA,则可能导至5.8%的患有CHD的整倍体胎儿得不到基因诊断。因此,对于胎儿CHDs,特别是伴有其他结构畸形,应考虑ES,因为基因诊断会显著影响新生儿结局。未来的研究需要为所有患有CHD的胎儿提供ES,以获得更可靠的估计。 |
声明:
1、凡本网注明“来源:小桔灯网”的所有作品,均为本网合法拥有版权或有权使用的作品,转载需联系授权。
2、凡本网注明“来源:XXX(非小桔灯网)”的作品,均转载自其它媒体,转载目的在于传递更多信息,并不代表本网赞同其观点和对其真实性负责。其版权归原作者所有,如有侵权请联系删除。
3、所有再转载者需自行获得原作者授权并注明来源。
 /3
/3 