
由于测序技术和数据分析的突破,遗传病的诊断技术正在发生革命性的改变。利用基因组学改变临床医学的潜力很大,特别是在罕见疾病领域。罕见病是一个庞大的、异质性的诊断群体,包括8000多种不同的疾病类型,其中绝大多数是遗传性的。每一种疾病都是罕见的,但当作为一个群体考虑时,罕见疾病又是常见的,总患病率约为6-8%。
罕见疾病的患病率变化很大。这些疾病中的有一些疾病相对常见,患病率超过1/20,000,而绝大多数是非常罕见的。这些疾病的临床表现多种多样,从仅影响身体很小一部分的轻度特征到涉及多个器官系统的严重表现。神经系统常受影响,导至智力残疾(ID)、神经精神疾病、癫痫(EP)和运动功能障碍等症状。发病年龄从产前到中老年不等,据估计,一半的病例是由儿科医生发现的。许多罕见疾病会导至慢性残疾,对患者及其家庭的生活以及医疗保健系统产生重大影响。为了优化治疗和护理以及关于预后和复发风险的遗传咨询,建立特异性诊断是至关重要的。对于许多疾病,比如先天代谢缺陷(IEM),治疗的形式是给予患者特定的饮食,重组酶治疗,小分子药物治疗等。在疾病早期阶段开始治疗有时可预防严重残疾或早期死亡,因此必须进行快速诊断。基因组测序需要的基础设施和专业知识超出了公共医疗资金的范围,因此严重依赖学术界。生命科学实验室(SciLifeLab)是由瑞典政府资助的国家基础设施,旨在通过技术平台提供高通量的生物科学,包括大规模平行测序(MPS)。SciLifeLab成立于2010年,是由四所大学共同努力建立的:卡罗林斯卡学院、瑞典皇家理工学院、斯德哥尔摩大学和乌普萨拉大学。当前,SciLifeLab支持瑞典所有主要大学的研究活动。许多国际基因组中心已经建立,几个大型的国际和国家测序项目已经启动,但临床整合却相对滞后。为了将基因组学整合到罕见疾病的医疗保健中,创建了卡罗林斯卡基因组医学中心-罕见病(GMCK-RD),这是SciLifeLab临床基因组学设施与斯德哥尔摩地区公共医疗之间的学术-临床合作,以便于在罕见病诊断中实施全基因组测序(WGS)。在公共医疗中使用学术基础设施并不存在先例,因为这两种治理体系是完全不同的。尽管存在上述挑战,一个完整的转化环境已经建立,其中生物信息学工具、工作流程和决策支持系统由多学科团队不断开发和改进,包括广泛的技术、实验和临床专业知识。这使得基因组数据的个性化分析、共享和解读成为可能,并通过卡罗林斯卡大学医院(Karolinska University Hospital)的三个不同机构(临床遗传学、遗传代谢疾病中心和临床免疫学)对不同疾病群体进行快速临床转化。我们报告了自2015年年中以来在Karolinska-Rare Diseases基因组医学中心(GMCK-RD)进行全基因组测序(WGS)的4437个人(3219名患者和1218名亲属)的研究结果。GMCK-RD的跨临床工作被组织成专门的团队,其中变异的解读由临床实验室遗传学家和来自GMCK-RD三个机构的在其特定领域的专家一起执行。1、着重于分析与病人疑似疾病相关的变异。为此,基因组数据首先在计算机上根据病人的表型被筛选出预先设定的临床相关基因包。分析一般都是单例进行的,但是对于具有高度异质性的复杂表型的患者,一般都需要进行家系分析。对于这样的病例,就需要分析大量的基因,比如包含3959个基因的整个OMIM疾病基因包。Trios也适用于新发变异比例高的疾病,如婴儿癫痫。2、在适当的时候,数据可以被GMCK-RD中的另一个团队共享和重新分析。这对于具有涉及多个医学领域更为复杂的临床症状的病人来说显得尤为重要。3、如果分子诊断并未找到明确的病因,但是仍然高度怀疑患有罕见遗传性疾病,这时候应该为病人/家属提供考虑全基因组检测的研究背景分析。直到2019年,从WGS分析中报告的所有变异均使用第二种方法进行验证:SNVs和INDELs,采用Sanger测序;缺失/重复 (> 50 bp),使用MLPA、微阵列或断点连接PCR。每个小组都需要进行跨学科的轮转。结果需要报告给相关的医生并且对于阳性结果需要向病人/家属提供遗传咨询。由于每个小组都有不同学科的相关临床专家,因此可以将遗传发现转化为个体化治疗。对于阴性结果,对罕见遗传病的怀疑仍然很高,如果高度怀疑为更严重的疾病,建议在6-12个月内重新转诊,否则建议在3-5年内重新分析基因组数据。为了确保高质量的分析,整个临床诊断中实施的工作流程都是具有高质量保证的。首先,数据生成和生物信息工作流程是ISO认证的,所有生物信息工具和过程都是按照规定的版本执行的。其次,使用参考材料和对先前分析的具有特定遗传畸变的一组代表性病例的再分析来验证工作流程中的每个变化。在2015-2019年期间,GMCK-RD分析了3219名患者的WGS数据。这期间,随着时间的推移,被分析的患者数量呈上升趋势(图1)。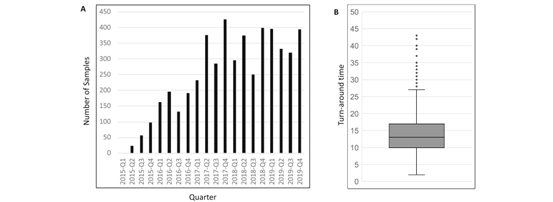
图1A 2015年至2019年每季度由GMCK-RD WGS测序的基因组DNA个体数;1B 测序的时间从2天到43天不等,中位数为13天其中分析的单个样本占84%,以家系进行分析的占16%,并且“基于表型的基因包”占92%,“OMIM基因包”占8%,这就意味着大部分的样本是以基于表型特异性基因包的单个样本进行分析的。对于所有病例来说,得到相应的分子诊断的为1285个,诊断率约为40%。单个病例检测的诊断率为34%,以家系进行检测的诊断率为36%。“基于表型的基因包”的诊断率为35%,“OMIM基因包”的诊断率为41%。通过更新版本的MIP(the MutationIdentification Pipeline framework )和基因包对WGS数据进行重新分析,诊断率得到了提高。对于不同的基因包诊断率在19%-54%之间(表1)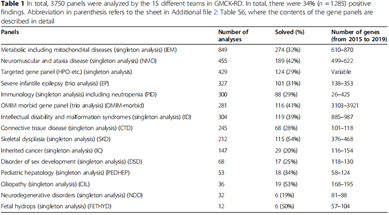
在1293个阳性报告中,致病基因具有异质性,甚至对于特定的变异位点也具有异质性。然而,一些基因是反复出现的,而且,一些致病变异也被证明在多个病例中反复出现。总共报告了754个不同疾病基因的变异,最常见的是COL2A1和FKRP,其次是MECP2和DYNC1H1。在本研究中COL1A2,COL5A1, FBN1, KCNQ2, STXBP1, ARID1B, RYR1以及 SCN1A都比较常见。但是对于大部分致病性基因来说,报告的变异仅在一个病人中检测到。有许多致病性变异在很多不相关的个体中被检测到。其中一些变异是已知的起因变异,比如FKRP基因中的c.826C>A, p.(Leu276Ile)以及RFC中的AAGGG重复,在12例肢带肌营养不良(LGMD2I)患者和5例CANVAS患者中分别以纯合子的状态被检测出来。另外也有显性遗传病相关的变异被检测到,比如TIA1基因中的c.1150G>A,p.(Glu384Lys) 以及TTR基因中的c.148G>A, p.(Val50Met),分别会导至常染色体显性遗传疾病Welander远端肌病以及遗传性淀粉样变性。除了起因变异,另外一些反复发现的变异也会在一些看起来不相关的病例中被检测到。比如在两个病人中检测出了CAPN1基因的c.1969G>T,p.(Glu657*)纯合无义突变,该突变与常染色体隐性遗传痉挛性截瘫相关。也有一些病人中检测到的变异是新发的,并且在常染色体显性遗传相关的家庭中出现共分离,比如在6个病例中检测到的常见的PRRT2基因中的c.694dup, p.(Arg217Profs*8)致病性变异,该基因会导至癫痫,另外在两个多发性外生骨疣的患者中分别检测出EXT1基因的c.1018C>T,p.(Arg340Cys)以及c.1018C>G,p.(Arg340Gly)。c.1018C>G变异是嵌合型的。同时还发现在不相关的病例中存在相同的会导至常染色体显性疾病的罕见变异,比如CHD7中的c.2504_2508del,p.(Tyr835Serfs*14),IFITM5(c.-14C>T)等。(表2)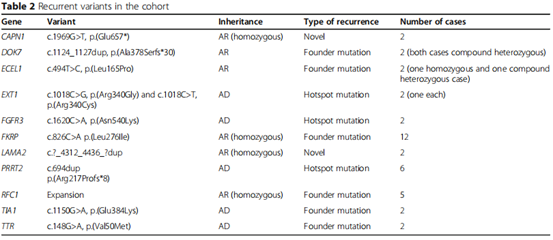
2017年,在基因包检测中引入了结构变异的检测;2019年,需要WGS能够检测出全基因组UPD,并进行STR分析(图2)。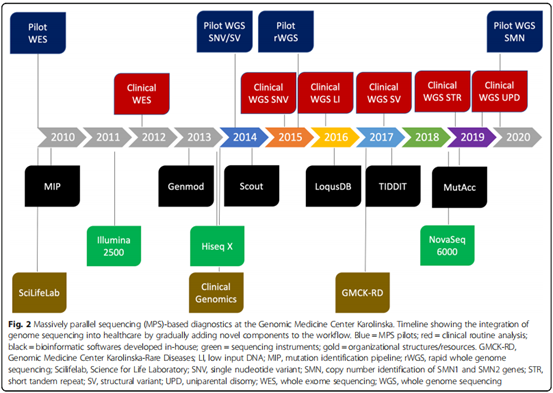
在检测出的1285个阳性病例中,其中870例可以确定遗传方式。最常见的遗传模式是常染色体隐性遗传,占468例,新发的占235例,107例为常染体显性遗传,48例为X连锁,线粒体遗传的占11例。在临床检测中,一代测序是最常用于大规模平行测序检测出来的SNVs及INDELS的验证的。尽管一代测序是一种可信度比较高的检测方式,但其价格昂贵并且费时。为了探索是否可以建立允许跳过Sanger测序的标准,对总共721个用Sanger测序分析的变异进行回顾性评估。在这721个变异中,32个是假阳性,32个中有31个是indels。在这32个变异中,有一个单个碱基的替换的质控分数低于GATK的最大值99。排除了质控分数低于最大值的INDELs和SNVs后,就只剩下503个变异了。对于这些变异,使用GATK判定为通过的变异为493例。另外还需要通过GMCK-RD工作组确定这些SNVs在IGV上观察到有超过20个reads,并且这些变异不存在于片段性重复区域。使用这些标准,我们的目的是排除报告的假阳性结果,因此484个变异(67%)将不需要使用二次方法进行验证(表3)。
后续包含更多变异的重分析表明,只要满足以上标准的变异就可以不需要再进行二次验证。进行临床分析之后,仍然存在一些高度怀疑有遗传性疾病的病例找不到发病的原因。对于这些病例,需要在全基因组范围内对所有的基因进行分析。通过这种方式,找到了17个新型的致病性基因,并且已经报道了遗传模式或者是致病机制。为了帮助发现新的致病基因,GMCK-RD最近加入了国际数据共享计划。许多大规模的基因组测序项目正在全球范围内进行,但临床实施在很大程度上是滞后的。全外显子组和全基因组测序对遗传诊断产生了巨大的影响。直到最近,遗传诊断还仅限于通过核型分析或阵列分析等对染色体畸变进行检测。因此,重点一直集中在诸如不明确的畸形综合征和智力残疾等情况,以及已确定少量潜在致病基因的特定单基因疾病。基因组学从根本上改变了这种情况。目前已知的约有4200种不同的单基因致病基因,可导至所有临床学科、所有年龄的疾病,从潜伏的、慢性的到剧烈急性的疾病。将WGS纳入诊断工作为这些截然不同的临床情况提供了巨大的确诊可能性,但也带来了挑战。基因组测序的一个主要挑战是每个个体存在大量的变异,每个测序的患者可能会产生数百万个遗传变异。管理和解读与每个疾病表现相关的数据需要一个高度复杂的、多学科的工作流程。通过将分析限制在与每个患者的个别疾病表现或家族遗传模式相关的基因的罕见变异上,可以产生可供诊断团队评估的可控制数量的变异。高度专业化的临床医生对于最初患者检测类型的选择和详细的表型分型方面很重要,有助于指导使用最合适的基因包进行一线分析以及有助于产生基于HPO的基因包分析。尽管局限于特定的基因包,但临床意义未明的变异是常见的,而且没有算法可以精确预测这些变异的功能和在体内的相关性。详细的临床专业知识和额外的诊断检测有助于对这些变异的评估。对于一些疾病来说快速的、靶向的检测分析是特别重要的,比如先天性代谢异常相关的疾病,特定的治疗有时候可以阻止严重的并发症甚至可以挽救生命。举例来说就是,在疑似急性发病的IEM患者中,通常在确诊之前会提供常规治疗。包括葡萄糖输注阻断分解代谢,减少潜在的有毒中间体,防止细胞能量不足。然而,丙酮酸脱氢酶缺乏症(PDHD)可引起急性或间歇性脑病并伴有严重的神经后遗症,葡萄糖输注是有害的而不是有益的。PDHD可能由至少六种不同的基因引起,应该通过限制碳水化合物和生酮饮食来治疗。在我们报告的患者中,有9人被诊断为PDHD。这些都是以前未确诊的病例,但是显著改善其临床结局的机会已经错过。人类遗传变异极为多样,从影响单个碱基对的小变异到影响数千或数百万个核苷酸的大结构变异。我们将不断发现影响编码区和非编码区的新型致病变异,并逐步了解不同变异的联合效应。随着我们对疾病遗传学的理解的扩展和新方法的可用性的提高,持续发展的环境确保了工作流程在不断地改进,使诊断率在这个迅速发展的领域持续改进。相对于外显子测序来说,WGS的主要优势是不仅可以分析SNVs和INDELS,还可以分析CNV,平衡的结构性变异,短散在重复序列等。我们最近发现WGS对平衡和不平衡的结构变异都有很高的检出率。在这里显示的数据中,只有一小部分病例被评估为结构变异和UPD。通过逐步分析,使用靶定基因包作为一线检测,下一步侧重于不同疾病组的互补团队之间进行咨询和数据共享,并在仍然没有诊断的病例中进行整个基因组的检测,就可以实现快速、严格的、高度专业化的分析和广泛的遗传筛选的综合价值。除了疾病基因的发现,在罕见病领域,以重组酶和其他生物制剂、小分子药物、反义技术、基因治疗和基因组编辑/细胞治疗等形式出现的新疗法也在大力发展。这种新疗法的使用将严重依赖于准确的诊断,既可以确定哪些患者可能受益,也可以避免那些不可能受益的患者使用。本研究表明,通过在综合临床-学术环境中应用临床WGS标准化工作流程,我们在广泛的表型亚群中实现了19-54%的诊断率。目前在医疗保健中大规模使用WGS面临的挑战包括需要澄清的实际问题和法律问题,以及关键资源如OMIM和HPO的限制。更新基因-表现型数据库非常重要。最后,随着需求的增加,重要的是要建立可持续的结构,将医疗保健和学术界连接起来,而不是严重依赖于努力创建合作的关键个人。我们表明,通过建立一个高度专业化的医生与训练有素的临床分子遗传学家和实验室医学、基因组学和生物信息学专家密切合作的环境,已经创建了一个可以持续学习的环境。这产生了强大的协同作用,使临床医学处于更好的位置,以跟上正在进行的快速科学和技术的发展。因为这需要在医疗保健内部以及医疗保健和学术界之间跨学科工作的全新方法,需要努力重组学术医学,减少孤立工作,实现数据和专业知识的共享。如果这一点能够实现,并且这个概念能够得到巩固和传播,那么我们正在朝着精准医疗采取决定性的步骤。临床WGS已经被证明是罕见疾病领域真正的改变者。在GMCK-RD的最初几年,> 1200名患者接受了在MPS技术开发之前无法在同一时间框架内实现的特异性分子诊断。这对患者及其家属产生了极大的影响,为他们的疾病提供了解释,并且结束了漫长的诊断过程。此外,还为患者及其家属提供了遗传咨询、预后信息和特殊治疗。
王小艳,湖北省妇幼保健院检验科遗传室,13年硕士研究生毕业于中南大学医学遗传学国家重点实验室 |
 /3
/3 