在抗体药领域,日本中外制药(Chugai)从成立到现在一直在不断创新。
从20世纪90年代的人源化抗体到2005年ADCC和ADCP增强型抗体到2008年的双特异抗体,循环抗体和清除抗体再到2012年Switch antibody直至现在的第三代双特异抗体,其每一次的创新都在解决抗体药领域中不同的难题。
可谓,低调的中外制药正在打造抗体工程平台的“航空母舰”。
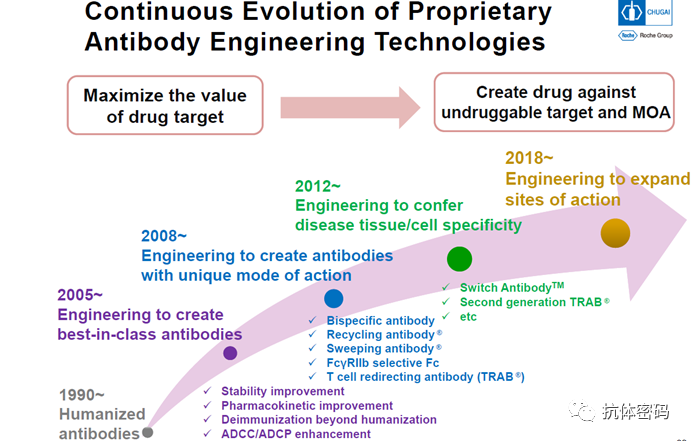
中外制药抗体技术的发展
本文从其技术平台切入。
ART-Ig为不对称1+1型的双特异抗体,为了防止两个结合不同抗原的Fab的轻链错配,其采用了共同轻链的策略。
共同的轻链的筛选方法如下图:首先筛选能够结合不同抗原的两个抗体,分别得到两个不同的轻链(每个轻链包含三个不同的CDR区),然后将两个不同抗体抗的CDR区进行组合,并利用体外实验对不同的组合进行评价,最终得到能够和两个不同重链互补配对且有生物学功能的轻链。 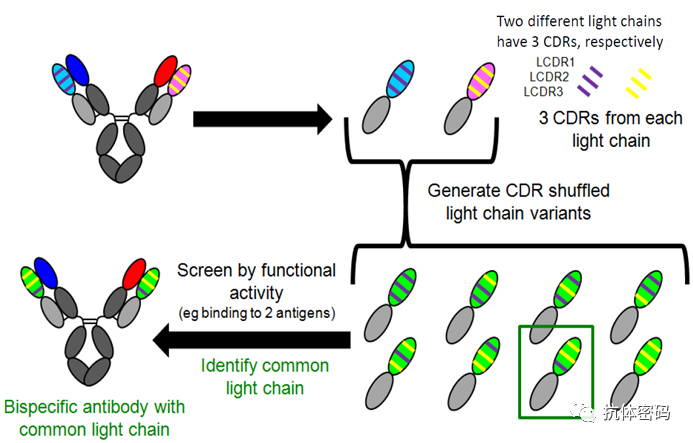
ART-Ig共同轻链筛选策略
为了防止抗体重链的错配,ART-Ig平台中对两个抗体的Fc 进行氨基酸突变,在其中一个抗的Fc端引入正电荷突变,在另外一个抗体的Fc端引入负电荷氨基酸突变。最终利用正负电荷相互吸引的特点促进两个不同的抗体正确配对,经过改造后,异源二聚体的比例高达99%。
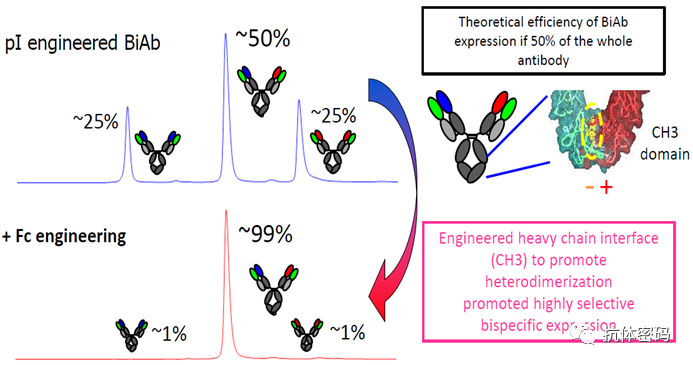
ART-Ig Fc正负电荷突变防止重链错配
虽然通过共同轻链和Fc引入正负电荷可以在很大程度上降低双特异抗体的错配,但是在生产中,错配问题不可避免,为了在下游纯化中除去错配的双特异抗体,ART-Ig对双特异抗体的两个抗体Fab的可变区进行氨基酸突变,使两个Fab有不同的等电点。
改造后正确配对的双特异抗体和错误配对的双特异抗体有不同的PI,因此在下游纯化中可以利用离子交换色谱柱除去错位配对的抗体。

ART-Ig PI改造通过纯化除去错配抗体
ART-Ig通过共同轻链防止抗体重链与轻链的错配,其生产工艺虽然方便,但是并在筛选共同轻链时难度较大。
FAST-Ig(Four-chain Assembly by electrostatic SteeringTechnology)与ART-Ig不同,为了降低双特异抗体中的轻链错配,在抗体的重链和轻链上都引入带电荷的氨基酸:在一个抗体的轻链引入负电荷,在对应的重链上引入正电荷;在另外一个Fab上通过氨基酸突变引入与第一个Fab相反的电荷。为了防止双特异抗体的重链错配,其技术方案与ART-Ig相同。
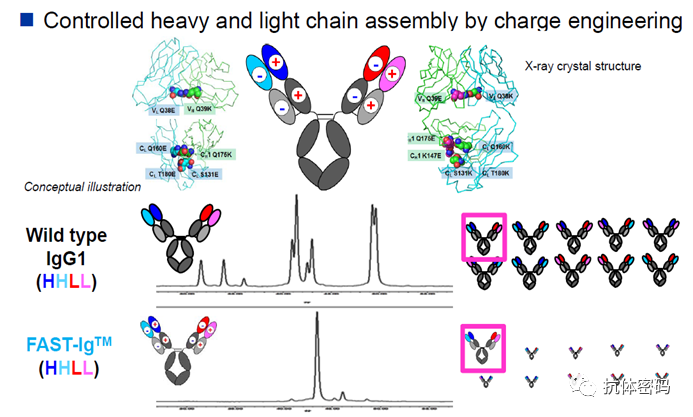
FAST-Ig引入不同电荷防止抗体轻链错配
第三代双特异抗体与以往的双特异性抗体不同,在抗体形式上与单克隆抗体相同,但是该抗体可以结合两种不同的抗原,即一个Fab可以结合两种不同的抗原,但是这两种抗原相互竞争。
抗体结合A抗原的时候无法结合B抗原,结合B抗原的时候无法结合A抗原,但是抗体无法同时结合A,B两种抗原。
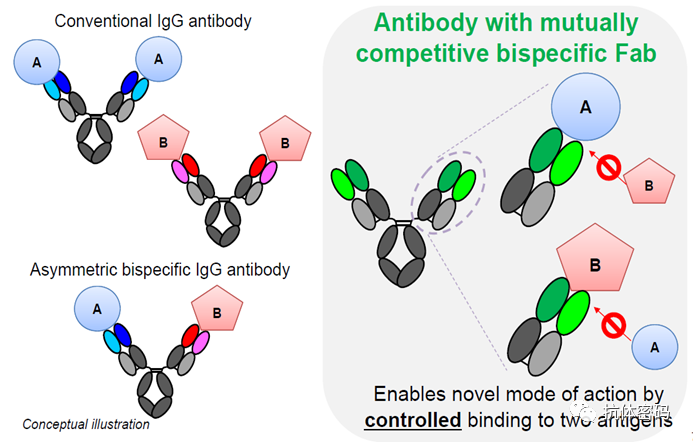
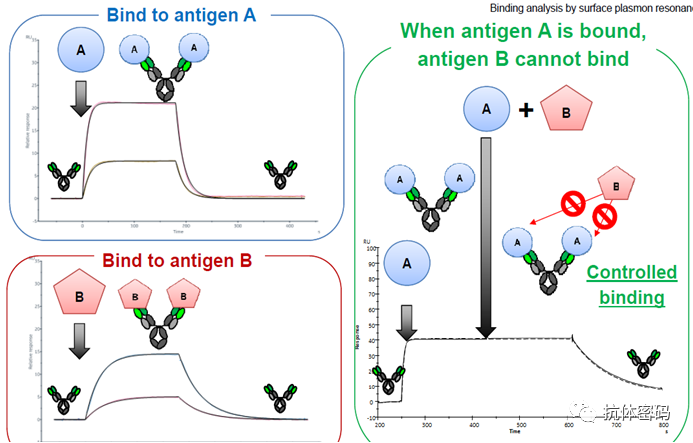
第三代双特异抗体作用示意图
在生物体内,抗体对抗原的清除主要是抗体结合抗原后,抗体抗原的复合物被细胞内吞后进入细胞,在细胞内,抗体抗原复合物被溶酶体降解,或者与FcRn结合后被带到细胞表面被释放到细胞外,因此,抗体对抗原的结合是一次性的。
而Recycling antibody是对抗体的可变区进行改造(主要是通过将抗体的CDR区的部分氨基酸替换为组氨酸),使抗体在PH7.4(中性环境)中结合抗原,而在PH6.0(溶酶体的酸性环境)中释放抗原。
当Recycling antibody抗体抗原复合物进入细胞溶酶体中后通过溶酶体降解或者释放后的抗原被溶酶体降解,而抗体通过FcRn再循环到细胞外,在细胞外,抗体可以再次结合抗原,因此可以多次重复利用,降低抗体相关药物的用量。
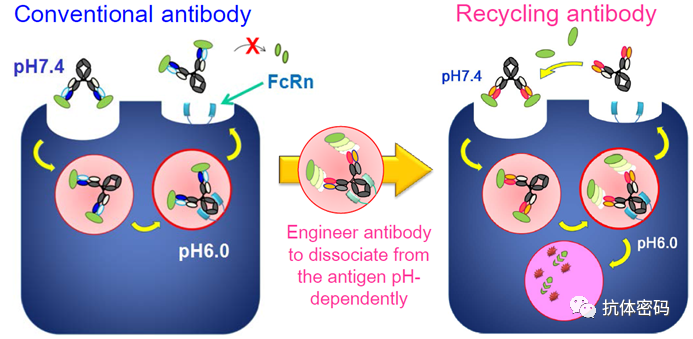
Recycling antibody抗体平台作用原理
是对Recycling antibody平台的进一步改造,改造后的抗体在中性条件下可以结合细胞膜表面的FcRn。
这样,抗体在结合抗原后可以很快的与细胞表面的FcRn结合被胞吞进入细胞,随后进入溶酶体降解,或者通过FcRn再循环回到细胞外。在生理条件下,抗体抗体被胞吞进入细胞速率较低,因此该机制可以加快抗体进入细胞,因此可以加快抗体对抗原的清除。
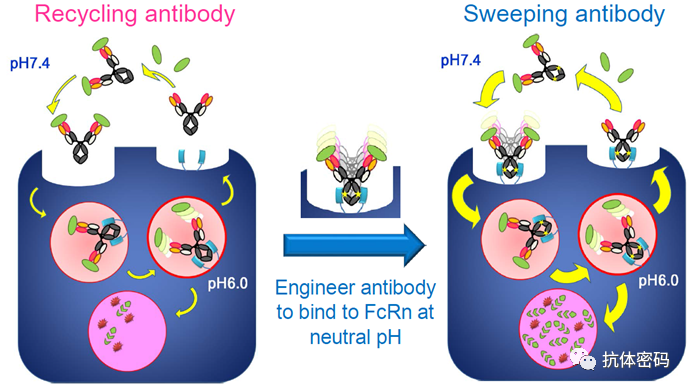
Sweeping antibody抗体平台作用机制
第一代的Sweeping antibody抗体在小鼠体内可以将抗原的清除能力提高约50倍,但是在猴子体内,其效果较差。为了能够使Sweeping antibody抗体在人体内发挥作用,中外制药引入了TwoB-Ig®和pI-FcTM技术。

第一代Sweeping antibody在小鼠体内的效果
TwoB-Ig®是对抗体的Fc进行改造,使抗体与FcγRIIb的亲合力增加。FcγRIIb在肝窦内皮细胞清除抗体抗原复合物中发挥主要作用,因此增加FcγRIIb对抗体的亲和力可以加速抗体抗原复合物的清除。
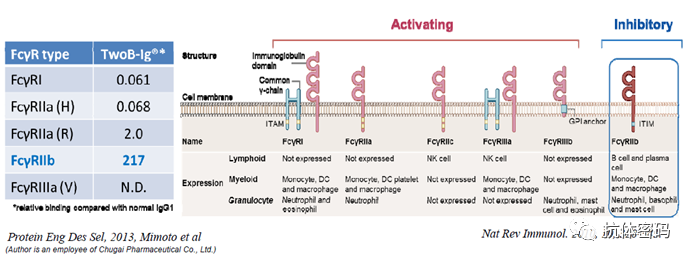
Fc与FcγRIIb的相互作用
pI-FcTM是利用细胞膜带负电的特性,对抗体的Fc改造,使其表面带更多的正电荷,当抗体与细胞膜接近时,通过抗体Fc的正电荷与细胞膜表面的负电荷的相互作用促进细胞对抗体抗原复合物的内吞。
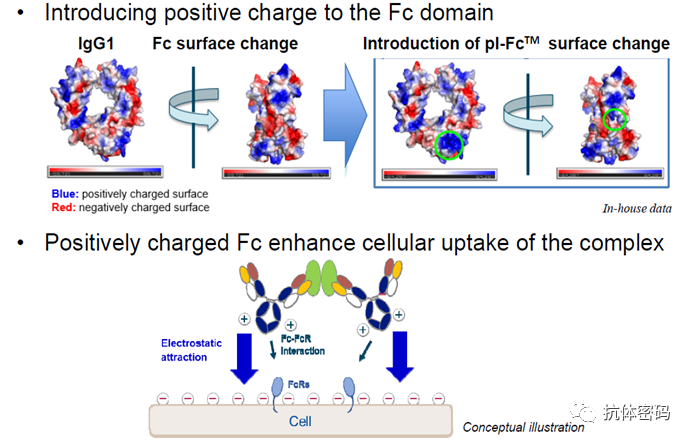
pI-FcTM作用机制示意图
经过改造后,新一代weeping antibody在猴子体内清除抗原的能力提高了约1000倍(下图粉红色线对应的抗体)。
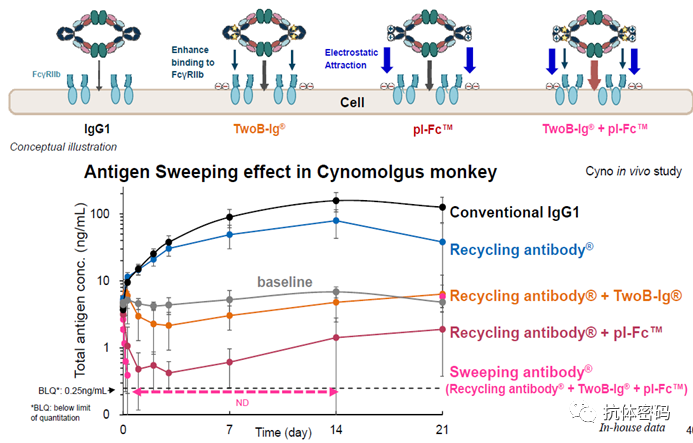
新一代weeping antibody在猴子体内对抗原的清除
Switch Antibody的开发主要是为了解决免疫治疗中的On-target 毒性问题。
对于激活机体免疫系统的抗体,如CTLA-4和4-1BB等抗体,其可以系统性的激活机体的免疫系统,从而导至过度的免疫反应;另外,靶向实体瘤的多种靶点在正常的细胞表面也会有表达,因此抗体可以无差别的结合肿瘤细胞上的靶点和正常细胞上的靶点,从而造成副反应。
而Switch Antibody利用某些小分子如ATP等在肿瘤微环境富集的特点,以小分子为媒介激活抗体,从而使抗体仅在肿瘤中特异性激活。
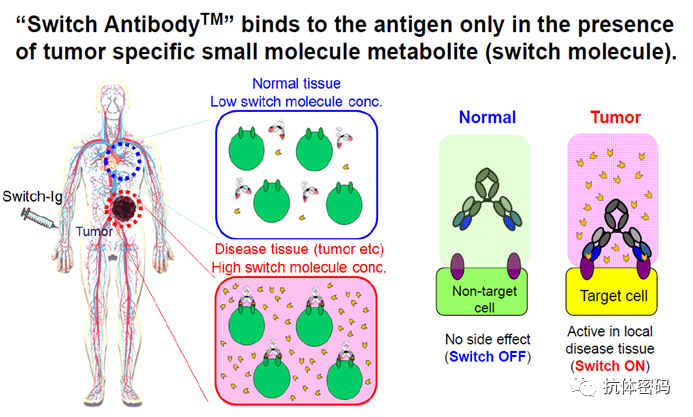
Switch Antibody作用示意图
中外制药选择的小分子为ATP,因为ATP在正在细胞内的浓度在5-8mM,在正常细胞外浓度约为30nM。但是在肿瘤微环境中,ATP会从坏死,凋亡等肿瘤细胞中释放,因此其浓度较高,有研究表明,在小鼠实体瘤中,其细胞外ATP浓度高于100uM。

ATP在小鼠肿瘤中的分布
相关阅读:Chugai制药神来之笔:肿瘤微环境抗体定向技术
ART-Fc(Asymmetric Re-engineering Technology-Fc)
ART-Fc是对抗体的两个Fc进行非对称的改造,以此来增强抗体Fc与FcγRIIIA的亲合力,从而增强抗体的ADCC效应。该方法比传统的去除岩藻糖增强ADCC的效果更好。 
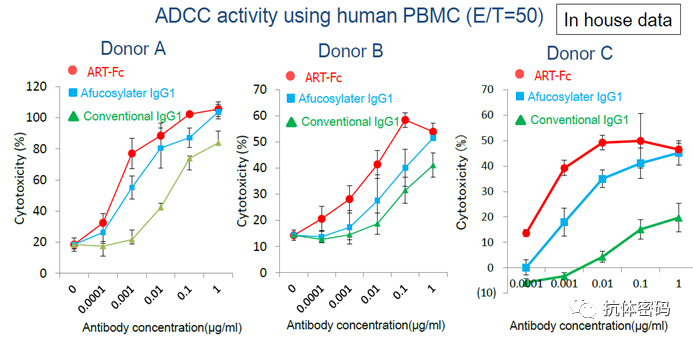
ART-Fc增强ADCC效果
ACT-Fc是通过对抗体的Fc改造,从而增强抗体与FcRn的结合能力,进而增加抗体的半衰期。传统抗体的半衰期在3周左右,改造后的抗体在Emicizumab上半衰期可以增加到50多天,这样理论上可以大大降低给药的频率。

ACT-Fc增加抗体的半衰期
ACT-Ig(Antibody Charge engineering Technology-Immunoglobulin)
ACT-Ig与ACT-Fc类似,都是增加抗体的半衰期,但是其改造方案却完全不同,ACT-Fc改造抗体的Fc增加抗体对FcRn的结合,而ACT-Ig是对抗体Fab的可变区进行改造,降低抗体的等电点(PI),使抗体在生理条件下带负电荷,因此与血管内皮细胞膜表面的负电荷相互排斥,进而降低抗体被细胞内吞,从而增加抗体的半衰期。
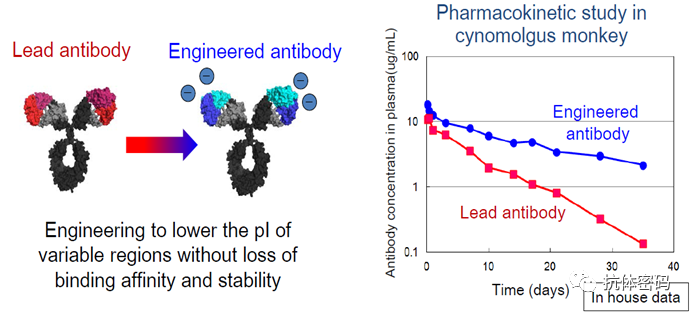
ACT-Ig的作用原理
在抗体发现平台方面,中外制药有兔B细胞筛选平台和独特的噬菌体筛选平台,两个平台都可以实现自动化高通量筛选。
兔单克隆抗体筛选平台可以筛选常规的抗体,其免疫原可以是DNA(类似于DNA疫苗,在兔体内表达抗原),蛋白或者细胞(适用于多次跨膜的膜蛋白)。噬菌体平台可以筛选有特殊需求且常规动物免疫无法获得的抗体,如Switch antibody等。

兔单抗和噬菌体筛自动化筛选平台
在高通量筛选的基础上,其在抗体的评价和优化上也实现了多个环节的高通量,如抗体设计,抗体转染(一周实现3000个抗体的转染),抗体纯化(一周实现1500个抗体的纯化),抗体多维度评价(亲合力,稳定性,溶解度,免疫原性和非特异性结合等评价)。
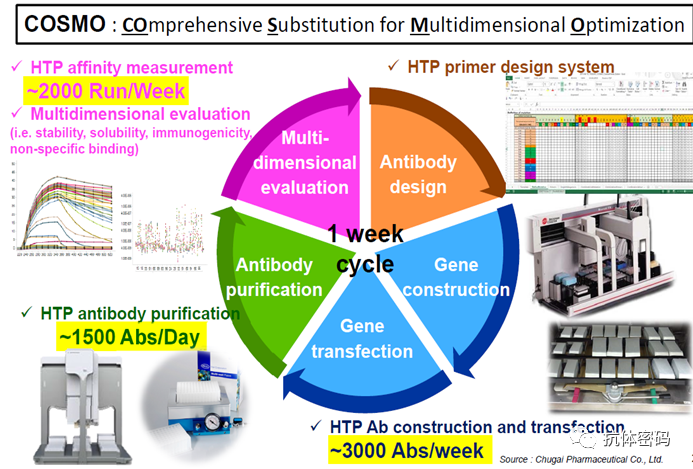
高通量抗体优化平台
经过工程化改造的抗体免疫原性是需要重点关注的一项指标。改造后的抗体首先需要利用T细胞检测其免疫原性,对于有免疫原性的抗体需要通过质谱检测可能存在免疫原性的序列,并利用计算机对其进行重新设计,并进行再次评估。
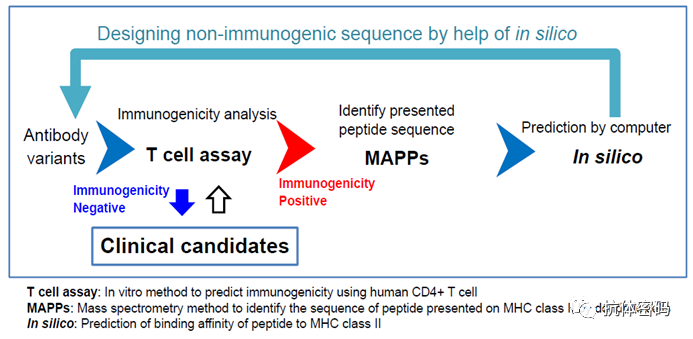
降低抗体免疫原性平台
中外制药的抗体相关技术平台几乎覆盖了抗体的方方面面。
从Sweeping抗体到循环性抗体,ADCC增强性抗体,再到延长半衰期型抗体,同时还有在肿瘤微环境特性激活的Switch-Antibody;在双特异抗体方面,其也在不停的更新换代,从ART-Ig到FAST-Ig再到目前的第三代双抗。
如果说中外制药是一艘航空母舰,那么我们国内的生物医药公司目前只是飘荡在长江中的货轮,但好在我们的一些医药公司也在逐渐增加研发创新投入,属于我们的医药界航母正在慢慢驶来!
*本文不构成任何投资,病人用药等建议。 |  /3
/3 