登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
Q:SDS-PAGE电泳的基本原理?
A:SDS-聚丙烯酰胺凝胶电泳,是在聚丙烯酰胺凝胶系统中引进SDS(十二烷基硫酸钠), SDS能断裂分子内和分子间氢键,破坏蛋白质的二级和三级结构,强还原剂能使半胱氨酸之间的二硫键断裂,蛋白质在一定浓度的含有强还原剂的SDS溶液中,与SDS分子按比例结合,形成带负电荷的SDS-蛋白质复合物,这种复合物由于结合大量的SDS,使蛋白质丧失了原有的电荷状态形成仅保持原有分子大小为特征的负离子团块,从而降低或消除了各种蛋白质分子之间天然的电荷差异,由于SDS与蛋白质的结合是按重量成比例的,因此在进行电泳时,蛋白质分子的迁移速度取决于分子大小。当分子量在15KD到200KD之间时,蛋白质的迁移率和分子量的对数呈线性关系,符合下式:logMW=K-bX,式中:MW为分子量,X为迁移率,k、b均为常数,若将已知分子量的标准蛋白质的迁移率对分子量对数作图,可获得一条标准曲线,未知蛋白质在相同条件下进行电泳,根据它的电泳迁移率即可在标准曲线上求得分子量。
Q:配胶缓冲液系统对电泳的影响?
A:在SDS-PAGE不连续电泳中,制胶缓冲液使用的是Tris-HCL缓冲系统,浓缩胶是pH6.7,分离胶pH8.9;而电泳缓冲液使用的Tris-甘氨酸缓冲系统。在浓缩胶中,其pH环境呈弱酸性,因此甘氨酸解离很少,其在电场的作用下,泳动效率低;而CL离子却很高,两者之间形成导电性较低的区带,蛋白分子就介于二者之间泳动。由于导电性与电场强度成反比,这一区带便形成了较高的电压剃度,压着蛋白质分子聚集到一起,浓缩为一狭窄的区带。当样品进入分离胶后,由于胶中pH的增加,呈碱性,甘氨酸大量解离,泳动速率增加,直接紧随氯离子之后,同时由于分离胶孔径的缩小,在电场的作用下,蛋白分子根据其固有的带电性和分子大小进行分离。
所以,pH对整个反应体系的影响是至关重要的,实验中在排除其他因素之后仍不能很好解决问题的情况,应首要考虑该因素。
Q:样品如何处理?
A:根据样品分离目的不同,主要有三种处理方法:还原SDS处理、非还原SDS处理、带有烷基化作用的还原SDS处理。
1、还原SDS处理:在上样buffer中加入SDS和DTT(或Beta巯基乙醇)后,蛋白质构象被解离,电荷被中和,形成SDS与蛋白相结合的分子,在电泳中,只根据分子量来分离。一般电泳均按这种方式处理,样品稀释适当浓度,加入上样Buffer,离心,沸水煮5min,再离心加样。
2、带有烷基化作用的还原SDS处理:碘乙酸胺的烷基化作用可以很好的并经久牢固的保护SH基团,得到较窄的谱带;另碘乙酸胺可捕集过量的DTT,而防止银染时的纹理现象。100ul样品缓冲液中10ul 20%的碘乙酸胺,并在室温保温30min。
3、非还原SDS处理:生理体液、血清、尿素等样品,一般只用1%SDS沸水中煮3min,未加还原剂,因而蛋白折叠未被破坏,不可作为测定分子量来使用。 
Q:SDS-PAGE电泳凝胶中各主要成分的作用?
A:聚丙烯酰胺的作用:丙烯酰胺与为蛋白质电泳提供载体,其凝固的好坏直接关系到电泳成功与否,与促凝剂及环境密切相关;
制胶缓冲液:浓缩胶选择pH6.7,分离胶选择pH8.9,选择tris-HCL系统,具体作用后面介绍;
TEMED与AP:促凝作用,加速聚丙烯酰胺的凝固;
十二烷基硫酸钠(SDS):阳离子去污剂,作用有四:去蛋白质电荷、解离蛋白质之间的氢键、取消蛋白分子内的疏水作用、去多肽折叠。
Q:提高SDS-PAGE电泳分辨率的途径?
A:1、聚丙烯酰胺的充分聚合,可提高凝胶的分辨率。建议做法:待凝胶在室温凝固后,可在室温下放置一段时间使用。忌即配即用或4度冰箱放置,前者易导至凝固不充分,后者可导至SDS结晶。一般凝胶可在室温下保存4天,SDS可水解聚丙烯酰胺。
2、一般常用的有氨基黑、考马斯亮蓝、银染色三种染料,不同染料又各自不同的染色方法,具体可参照郭尧君编著的《蛋白质电泳技术手册》P82-103。 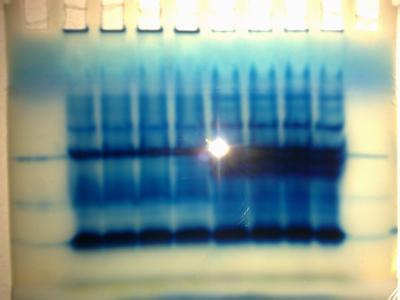
Q:“微笑”(两边翘起中间凹下)形带原因?
A:主要是由于凝胶的中间部分凝固不均匀所致,多出现于较厚的凝胶中。
处理办法:待其充分凝固再作后续实验。
Q:“皱眉”(两边向下中间鼓起)形带原因?
A:主要出现在蛋白质垂直电泳槽中,一般是两板之间的底部间隙气泡未排除干净。
处理办法:可在两板间加入适量缓冲液,以排除气泡。
Q:为什么带出现拖尾现象?
A:主要是样品融解效果不佳或分离胶浓度过大引起的。
处理办法:加样前离心;选择适当的样品缓冲液,加适量样品促溶剂;电泳缓冲液时间过长,重新配制;降低凝胶浓度。
Q:为什么带出现纹理现象?
A:主要是样品不溶性颗粒引起的。
处理办法:加样前离心;加适量样品促溶剂。
Q:什么是“鬼带”,如何处理?
A:“鬼带”就是在跑大分子构象复杂的蛋白质分子时,常会出现在泳道顶端(有时在浓缩胶中)的一些大分子未知条带或加样孔底部有沉淀,主要由于还原剂在加热的过程中被氧化而失去活性,致使原来被解离的蛋白质分子重新折叠结合和亚基重新缔合,聚合成大分子,其分子量要比目标条带大,有时不能进入分离胶。但它却于目标条带有相同的免疫学活性,在WB反应中可见其能与目标条带对应的抗体作用。
处理办法:在加热煮沸后,再添加适量的DTT或Beta巯基乙醇,以补充不足的还原剂;或可加适量EDTA来阻止还原剂的氧化。
Q:为什么溴酚蓝不能起到指示作用?
A:我们在实验中常会遇到溴酚蓝已跑出板底,但蛋白质却还未跑下来的现象。主要与缓冲液和分离胶的浓度有关。
处理办法:更换正确pH值的Buffer;降低分离胶的浓度。
Q:为什么电泳的条带很粗?
A:电泳中条带很粗是常见的事,主要是未浓缩好的原因。
处理办法:适当增加浓缩胶的长度;保证浓缩胶贮液的pH正确(6.7);适当降低电压;
Q:为什么电泳电压很高而电流却很低呢?
A:这种现象一般初学者易出现。比如电压50v以上,可电流却在5mA以下。主要是由于电泳槽没有正确装配,电流未形成通路。包括:a.内外槽装反;b.外槽液过少;c.电泳槽底部的绝缘体未去掉(比如倒胶用的橡胶皮)。
处理办法:电泳槽正确装配即可。
Q:浓缩胶与分离胶断裂、板间有气泡对电泳有影响吗?
A:这主要出现在初学者中,一般对电泳不会有太大的影响。前者主要原因是拔梳子用力不均匀或过猛所致;后者是由于在解除制胶的夹子后,板未压紧而致空气进入引起的。
处理办法:按正确的操作方法操作。
实验步骤:
1. 5x样品缓冲液(10ml):0.6ml 1mol/L的Tris-HCl(pH6.8),5ml 50%甘油,2ml 10%的SDS,0.5ml巯基乙醇,1ml 1%溴酚蓝,0.9ml蒸馏水。可在4℃保存数周,或在-20℃保存数月。
2. 凝胶贮液:在通风橱中,称取丙烯酰胺30g,甲叉双丙烯酰胺0.8g,加重蒸水溶解后,定容到100ml。过滤后置棕色瓶中,4℃保存,一般可放置1个月。
3. pH8.9分离胶缓冲液: Tris 36.3g ,加1mol/L HCl 48ml,加重蒸水80ml使其溶解,调pH8.9,定容至100ml, 4℃保存。
4. pH6.7浓缩胶缓冲液: Tris 5.98g ,加1mol/L HCl 48ml,加重蒸水80ml使其溶解,调pH6.7,定容至100ml, 4℃保存。
5. TEMED(四乙基乙二胺)原液。
6. 10%过硫酸铵(用重蒸水新鲜配制)。
7. pH8.3 Tris-甘氨酸电极缓冲液:称取Tris 6.0g,甘氨酸28.8g,加蒸馏水约900ml,调pH8.3后,用蒸馏水定容至1000ml。置4℃保存,临用前稀释10倍。
8. 考马斯亮蓝G250染色液:称100mg考马斯亮蓝G250,溶于200ml蒸馏水中,慢慢加入7.5ml 70%的过氯酸,最后补足水到250ml,搅拌1小时,小孔滤纸过滤。
器材:电泳仪,电泳槽,水浴锅,摇床。
样品制备:将蛋白质样品与5X样品缓冲液(20ul+5ul)在一个Eppendorf管中混合。放入100℃加热5-10min,离心,取上清点样。
电泳:
1. 将玻璃板、样品梳、Spacer用洗涤剂洗净,用ddH2O冲洗数次,再用乙醇擦拭,晾干;
2. 将两块洗净的玻璃板之间加入Spacer,装好玻璃板;
3. 按如下体积配制10%分离胶8.0 ml,混匀;
4. 向玻璃板间灌制分离胶,立即覆一层重蒸水,大约20 min后胶即可聚合;
按如下体积配制6%浓缩胶3.0 ml,混匀;ddH2O 1.0 mol/LTris-HClpH=6.8 30% ,
将上层重蒸水倾去
2.0 ml 400 ul 600 ul
10% SDS 10% AP TEMED
36ul 24ul 4ul
6. 滤纸吸干,灌制浓缩胶,插入样品梳;
7. 装好电泳系统,加入电极缓冲液,上样20 μl;
8. 稳压200V,溴酚蓝刚跑出分离胶时,停止电泳,约需45 min~1hr;
9. 卸下胶板,剥离胶放入染色液中,室温染色1~2 hr;加入脱色液,置于80 rpm脱色摇床上,每20 min更换一次脱色液(10 ml 冰乙酸;45 ml乙醇;45 ml蒸馏水)至完全脱净。
SDS-PAGE胶的干燥:
凝胶干燥时遇到的主要问题是凝胶的变形和破裂。将凝胶放在Whatman 3MM滤纸上可防止干燥凝胶变形,但凝胶是否破裂取决于凝胶的厚度和干燥器的质量,因此,应尽量使用薄胶并使凝胶干燥器处于良好状态,使其真空压力波动极少。
试剂配制步骤
1. 固定液:冰醋酸:甲醇:水(10:20:70)
2. 电泳后的凝胶用5~10倍体积固定液在室温下固定,酸性固定液扩散后可使凝胶中的溴酚蓝变黄。蓝色全部消失后,继续固定5min。为防止凝胶破裂,在进行此步骤之前可将凝胶浸泡于含20%甲醇、30%甘油的溶液中过夜。
3. 将凝胶标记好方向后放在保鲜膜或玻璃纸上面,上面放一张比凝胶四周长出1~2cm的Whatman 3MM滤纸。
4. 另将一张滤纸放在凝胶干燥器上。将Whatman 3MM滤纸/凝胶/保鲜膜或玻璃纸,放在凝胶干燥器上的滤纸上面,保鲜膜或玻璃纸在最上面。
5. 放下凝胶干燥器的盖子,抽真空使凝胶四周封闭以干燥凝胶,干燥时间常由厂家提供,一般0.75mm厚凝胶干燥2h,如50~65℃可加快干燥进程。
6. 释放真空。如加热状态下干燥,则先停止加热并自然冷却10min后再释放真空.
作者: 张冬琳 来源:人人网
|  /3
/3 