登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
近日,因美纳CN MiSeq™Dx五款测序反应通用试剂已获得药品监督管理局的一类体外诊断试剂备案(备案号:沪闵械备20250100)。

目前,因美纳在华获批的基因测序仪MiSeq™Dx1和NextSeq™ 550Dx2均拥有配套一类备案的国产测序反应通用试剂,为多种应用场景提供完整、便捷的本土化解决方案。
此次备案更新的五款测序反应通用试剂盒专为适配MiSeq™Dx基因测序仪而设计,具备灵活、稳定、高效的特点。
近日,腾讯医疗健康(深圳)有限公司的“认知功能训练软件”获二类医疗器械注册证(粤械注准20252210654)。
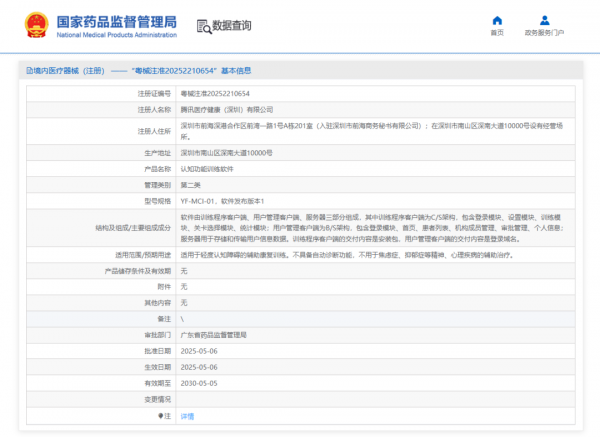
这款软件由腾讯多部门联合研发,中山大学心理学系指导,经临床试验验证,98%的受试者在12周训练后认知能力显著改善。这是腾讯第六张医疗器械注册证,覆盖多病种,标志着其在医疗科技领域的持续突破,推动“智慧康复”生态发展。
03 万泰生物与鸿宇泰达成战略合作,聚焦神经系统疾病体外诊断 6月23日,万泰生物与鸿宇泰生物正式签署战略合作协议,锚定神经系统疾病体外诊断领域。此次合作将深度融合双方优势,万泰生物凭借全产业链布局与全球化市场渠道,鸿宇泰生物依托神经疾病标志物检测核心技术,共同打造覆盖“早筛 - 诊断 - 监测”的精准医疗闭环。

双方将通过协同创新,提升低丰度生物标志物的检出能力,攻克核心原材料技术壁垒,构建“早筛 - 干预 - 监测”全周期解决方案,助力健康老龄化目标的实现,为3.1亿老年群体的健康护航。
2025年6月24日,复星医药召开股东会,完成董事会换届选举,并聘任新一届高级管理人员。陈玉卿任董事长,关晓晖任联席董事长,文德镛任副董事长;刘毅任CEO兼总裁,李静、王兴利、张文杰任联席总裁。新班子具备扎实的药械诊疗产业背景,将推动复星医药成为全球领先的医疗创新整合者。复星医药注重人才梯队建设,积极汇聚全球行业精英,未来将围绕未满足的临床需求,加快创新转型与全球化发展,为客户、员工、股东和社会创造更大价值。
2025年6月24日,国家药监局发布《免于进行临床试验体外诊断试剂目录(2025年)的通告(2025年第23号)》。此次修订对原2021年版目录进行了系统更新,旨在进一步规范体外诊断试剂注册流程,优化行业准入环境,降低企业研发和注册成本。新目录涵盖病原体检测、毒品检测、肿瘤标志物等数百个体外诊断试剂品种,涉及众多Ⅱ类和Ⅲ类产品,覆盖范围更广,技术成熟度更高。这一调整将帮助企业降本提效,提升产品迭代能力,推动体外诊断行业向标准化、差异化发展。 |
 /3
/3 