金桔
金币
威望
贡献
回帖0
精华
在线时间 小时
|
登陆有奖并可浏览互动!
您需要 登录 才可以下载或查看,没有账号?立即注册


×
前言
CAR-T疗法,即嵌合抗原受体T细胞免疫疗法,英文全称Chimeric Antigen Receptor T-Cell Immunotherapy,是一种治疗肿瘤的精准靶向疗法,近几年通过优化改良在临床肿瘤治疗上取得了很好的效果。其一般技术原理是通过基因工程技术,将T细胞激活,并装上定位导航装置CAR(肿瘤嵌合抗原受体),将T细胞改造成CAR-T细胞,利用CAR专门识别体内肿瘤细胞,并通过免疫作用释放大量的多种效应因子,高效地杀灭肿瘤细胞,从而达到治疗恶性肿瘤的目的[1]。
嵌合抗原受体T细胞是抗体的单链可变区域(scFv)与T细胞表面受体嵌合于T细胞上,形成的嵌合抗原受体主要由胞外区、跨膜区和胞内区域三部分组成。胞外区常为单链抗体(scFv),负责识别并结合靶抗原;跨膜区是铰链或间隔区,可将scFv锚定于细胞膜上;胞内信号域由共刺激因子和CD3信号域组成。当抗原被识别和结合后,产生刺激信号传至胞内信号域,T细胞被激活并发挥效应功能[2]。其中T细胞嵌合抗原受体的结构如图1所示。
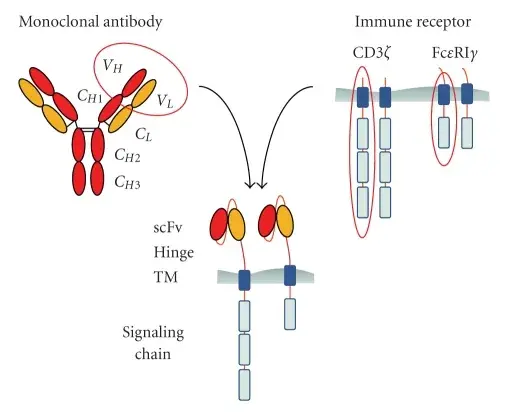
图1. CAR-T结构[3]
CAR与细胞表面上表达的靶抗原的结合不依赖于MHC受体,从而导致强有力的T细胞活化和强大的抗肿瘤反应。然而,CAR-T细胞疗法仍有重大的局限性必须解决,包括危及生命的CAR-T细胞相关毒性,对实体瘤疗效的有限性,B细胞恶性肿瘤中的抑制和抵抗性,抗原逃逸,有限的持久性,较差的迁移和肿瘤浸润,以及免疫抑制性微环境。全球范围内,CAR-T疗法安全问题一直是大家关注的焦点。除此之外,传统CAR-T疗法还面临以下痛点:生产制备流程复杂,耗时较长;在制备CAR-T细胞的同时,患者须接受化疗预处理,以提高CAR-T细胞注入后的疗效;有些患者因为身体健康水平,前期治疗等多种原因,无法提供足够的T细胞,导致他们不能从这一突破性技术中获益。
在2022年1月,一篇发表在Science期刊上文献系统性介绍了一种可在体内瞬时生成的CAR-T细胞的新疗法。与传统CAR-T疗法相比,这种新疗法的最大的特点是将身体本身变成了一个可以选择性重编程T细胞的工厂,而无需将T细胞取出体外进行编辑、培养后再输入体内。这种新疗法是利用具有靶向性的纳米脂质体(tLNP)将mRNA递送到T细胞进行重编程(见图2),将T细胞转化可以攻击心脏成纤维细胞的CAR-T细胞(FAP-CAR-T细胞)。该研究结果表明,瞬时产生的CAR-T细胞明显减少小鼠心脏的纤维化,并恢复了心脏的大小和功能[4]。,据报道,新型的tLNP可将编码抗CD19 CAR的mRNA有效载荷传递给表达CD8的T细胞,从而有效地在体内工程化CAR-T细胞。这种方法的治疗目标是通过将血液和淋巴组织中的B细胞快速深度清除来实现免疫系统的重置,而不受常规离体CAR-T的挑战[5]。如何准确地检测CAR-T细胞,对该疗法的研究至关重要。
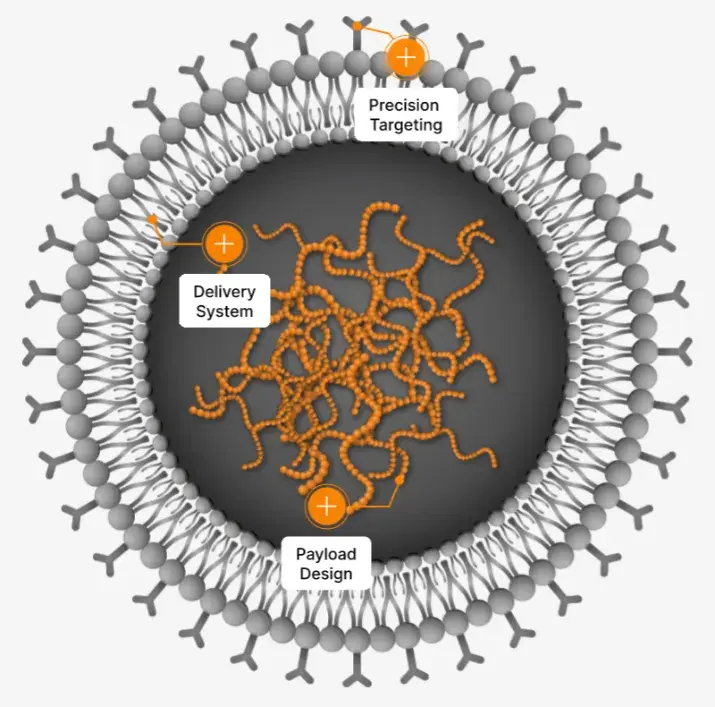
图2. T细胞靶向LNP递送系统[5]
流式细胞术检测CAR-T细胞
检测CAR-T细胞的技术包括成像技术、流式细胞术、免疫组化技术、定量PCR技术等,不同的方法适用于不同的检测样本和检测目的。其中,流式细胞术(flow cytometry)可用于获得细胞动力学曲线,测量单位体积血液中的CAR-T细胞数,相关细胞亚群百分比及细胞数的变化。基于这些优势,流式细胞数在CAR-T产品的临床前研究中被广泛的应用。以下是对流式细胞在CAR-T产品分析中应用场景的具体介绍。
1.荧光参比微球-绝对计数
利用荧光参比微球进行流式细胞仪绝对计数,为目前被临床及科研工作者广泛认可的流式细胞仪单平台绝对计数方法之一。在待测目的细胞悬液样本制备过程中,先将样本直接加入含已知绝对数量荧光参比微球的绝对计数管中,或者在流式管中加入与待测目的细胞悬液样本等体积、已知绝对数量的荧光参比微球,再加入用于标记待测目的细胞的抗体,待抗体标记后,混匀细胞悬液与荧光参比微球上流式细胞仪检测,同时记录目的细胞与荧光参比微球的计数结果(见图3)。两者在数量上存在一定的比例关系,根据荧光参比微球的计数结果与绝对数量即可换算出目的细胞的绝对计数值[6]。

图3.利用荧光参比微球的流式细胞仪单平台绝对计数方法的原理示意图
2.CAR-T细胞检测
根据CAR结构的不同,可以针对性的选择不同的检测抗体(见图4)。Whitlow/218肽是一种常用的连接单链可变片段(scFvs),利用细胞外scFv进行靶标抗原识别的嵌合抗原受体(CARs)的可变重链(VH)结构域和可变轻链(VL)结构域的链接器。在细胞外,Whitlow/218链接器(E3U7Q)赋予scFv增强的抗蛋白酶和抗聚集性,将与含有Whitlow/218链接器的scFv,以及具有不同特异性的细胞表面表达的CARs反应[7]。
除了Whitlow/218链接器外,多聚甘氨酸-丝氨酸(G4S)链接器是一种柔性、无结构的合成肽链接器序列,链接器本身由一个核心五肽序列,甘氨酸-甘氨酸-甘氨酸-甘氨酸-丝氨酸构成,在基于scFv的CARs和scFv片段中,重复并以15聚体(G4S)3或20聚体(G4S)4常见。链接器序列长度在控制scFv稳定性和VH与VL结构域之间的非共价结合中起作用[8,9]。
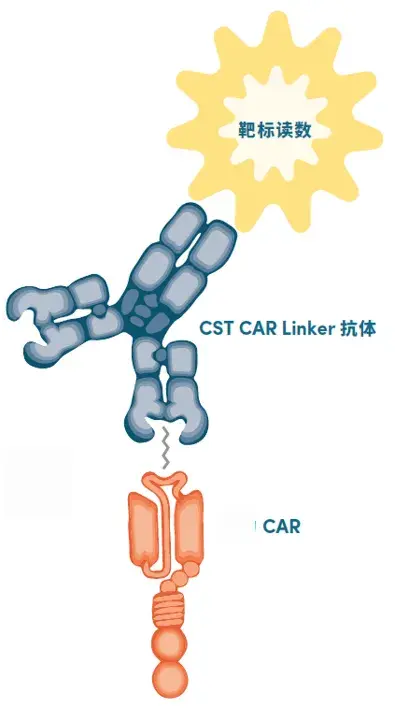
图4. CAR结构流式检测原理[10]
3.免疫表型分析
免疫表型是指对细胞群进行分析,以鉴定多种目标细胞群的存在及比例。该过程使用抗体进行鉴定,抗体可特异性检测这些细胞表达的抗原,即标记物。采用流式细胞术进行免疫表型是鉴定和分类复杂细胞群中细胞的首选方法。
免疫表型分析则可以根据使用动物模型的不同,对动物外周血、淋巴结、脾脏、骨髓等组织中的淋巴细胞进行表型分析(如CD45+、CD3+、CD4+、CD8+、CD20+、CD159+、CD14+等)。另外,根据CAR-T种类及作用的不同,如靶点为CD19的CAR-T细胞,可以清除带有CD19的癌变B细胞,分析时,通过不同的B细胞表面抗原(如CD19+、CD20+、CD21+、CD27+、IgD+等),将B细胞分为以下亚群11,进行B细胞清除的检测(见图5)。
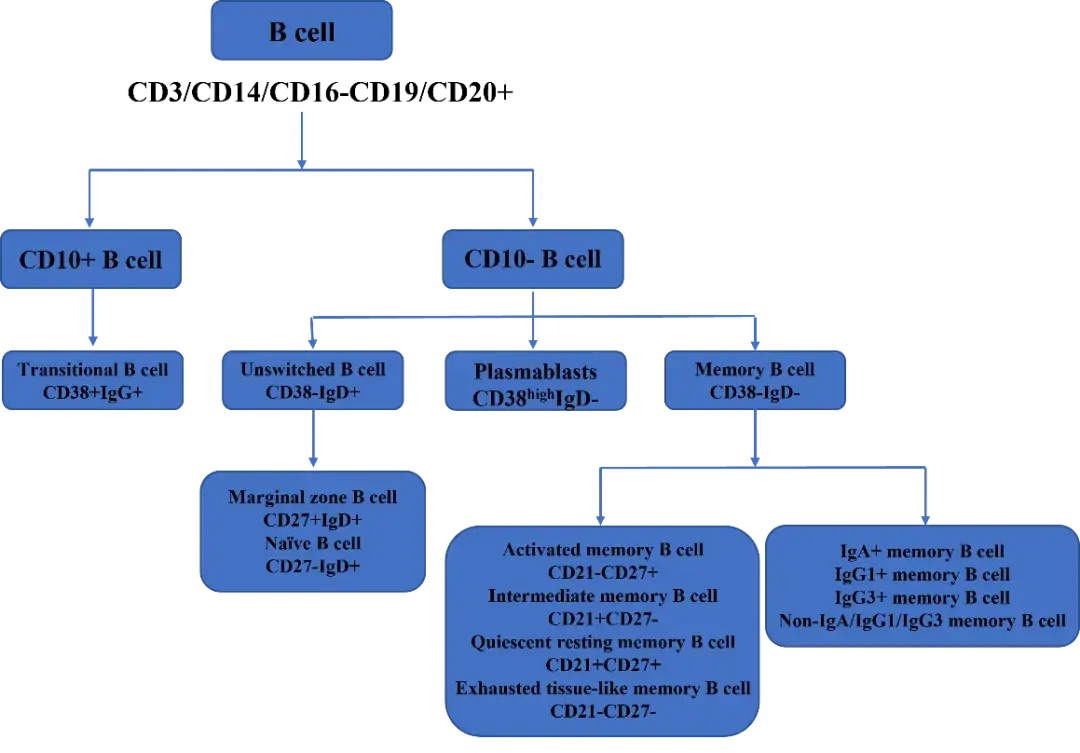
图5. B细胞清除流式分析
药明康德生物分析部流式分析平台能力
药明康德生物分析部搭建了全服务链的流式细胞术分析平台,开发和验证了多个免疫表型(IPT),受体占有率(RO)和细胞因子(CK)的生物分析方法,符合NMPA免疫毒性和GLP检测的指导原则,最新白皮书及文献要求,与国际接轨。该平台具有丰富的分析经验和先进的检测设备(5激光,18色)(见图6)。
药明康德生物分析部承接了大量的基因及细胞治疗产品的临床前和临床的安全性评价工作,包括基因治疗产品如腺病毒AAV类药物。检测方面,在人、食蟹猴、恒河猴、SD大鼠、Balb/c小鼠、巴马小型猪、比格犬中开发了多种不同细胞亚群组合的方法,包含T淋巴细胞,调节性T细胞,B淋巴细胞,自然杀伤细胞,单核细胞,树突状细胞,巨噬细胞,浆细胞等,可以对全血、PBMC、肝脏、脾脏、淋巴结、骨髓等多种不同种类的样本进行分析。包含的细胞表面标志物有CD3,CD4,CD8,CD11c,CD14,CD16,CD19,CD20,CD21,CD25,CD27,CD38,CD40,CD45,CD56,CD69,CD80,CD123,CD159,HLA-DR等,胞内抗体FoxP3和Ki-67,可以分析细胞活化,细胞增殖,细胞凋亡等各类参数。

图6.药明康德生物分析部流式细胞仪
药明康德生物分析部引进了一系列的自动化设备,包括流式细胞仪高通量检测模块,自动化液体工作站等,能够根据实验需求,为客户提供更优更经济的方法和方式。在多种自动化设备和多种仪器设备/模块的助力下,保证了实验室工作的高通量,高效率和高质量。
如果您想咨询相关业务或者对其他业务感兴趣,欢迎点击如下链接,联系我们
参考文献
Qi, C., Gong, J., Li, J. et al. Claudin18.2-specific CAR T cells in gastrointestinal cancers: phase 1 trial interim results. Nat Med 28, 1189–1198 (2022). https://doi.org/10.1038/s41591-022-01800-8
Chen YJ, Abila B, Mostafa Kamel Y. CAR-T: What Is Next? Cancers (Basel). 2023 Jan 21;15(3):663. doi: 10.3390/cancers15030663. PMID: 36765623; PMCID: PMC9913679.
https://www.cn-healthcare.com/articlewm/20210403/content-1206456.html
Rurik JG, Tombácz I, Yadegari A, Méndez Fernández PO, Shewale SV, Li L, Kimura T, Soliman OY, Papp TE, Tam YK, Mui BL, Albelda SM, Puré E, June CH, Aghajanian H, Weissman D, Parhiz H, Epstein JA. CAR T cells produced in vivo to treat cardiac injury. Science. 2022 Jan 7;375(6576):91-96. doi: 10.1126/science.abm0594. Epub 2022 Jan 6. PMID: 34990237; PMCID: PMC9983611.
https://www.capstantx.com/
Brando B, Barnett D, Janossy G, Mandy F, Autran B, Rothe G, Scarpati B, D'Avanzo G, D'Hautcourt JL, Lenkei R, Schmitz G, Kunkl A, Chianese R, Papa S, Gratama JW. Cytofluorometric methods for assessing absolute numbers of cell subsets in blood. European Working Group on Clinical Cell Analysis. Cytometry. 2000 Dec 15;42(6):327-46. doi: 10.1002/1097-0320(20001215)42:6<327::aid-cyto1000>3.0.co;2-f. PMID: 11135287.
Mare Whitlow, Brian A. Bell, Sheau-Line Feng, David Filpula, Karl D. Hardman, Steven L. Hubert, Michele L. Rollence, James F. Wood, Margaret E. Schott, Diane E. Milenic, Takashi Yokota, Jeffrey Schlom, An improved linker for single-chain Fv with reduced aggregation and enhanced proteolytic stability, Protein Engineering, Design and Selection, Volume 6, Issue 8, November 1993, Pages 989–995, https://doi.org/10.1093/protein/6.8.989
Huston JS, Levinson D, Mudgett-Hunter M, Tai MS, Novotný J, Margolies MN, Ridge RJ, Bruccoleri RE, Haber E, Crea R, et al. Protein engineering of antibody binding sites: recovery of specific activity in an anti-digoxin single-chain Fv analogue produced in Escherichia coli. Proc Natl Acad Sci U S A. 1988 Aug;85(16):5879-83. doi: 10.1073/pnas.85.16.5879. PMID: 3045807; PMCID: PMC281868.
Chen X, Zaro JL, Shen WC. Fusion protein linkers: property, design and functionality. Adv Drug Deliv Rev. 2013 Oct;65(10):1357-69. doi: 10.1016/j.addr.2012.09.039. Epub 2012 Sep 29. PMID: 23026637; PMCID: PMC3726540.
https://www.cellsignal.cn/
Liechti T, Günthard HF, Trkola A. OMIP-047: High-Dimensional phenotypic characterization of B cells. Cytometry A. 2018 Jun;93(6):592-596. doi: 10.1002/cyto.a.23488. Epub 2018 May 21. PMID: 29782066; PMCID: PMC6704361.
Verheul RC, JCT van Deutekom and NA Datson. (2016).
Digital droplet PCR for the absolute quantification of exon
skipping induced by antisense oligonucleotides in (pre-)-
clinical development for Duchenne muscular dystrophy.
PLoS One 11:e0162467
Verheul RC, JCT van Deutekom and NA Datson. (2016).
Digital droplet PCR for the absolute quantification of exon
skipping induced by antisense oligonucleotides in (pre-)-
clinical development for Duchenne muscular dystrophy.
PLoS One 11:e0162467
⤵️喜欢我们的内容,欢迎关注@药明康德市场部!或者点赞、评论、分享给其他读者吧!
原文地址:https://zhuanlan.zhihu.com/p/695277401 |
|
 /3
/3 