
青年千人计划专家 施奇惠教授
在癌症诊断与治疗中,医生通常依赖侵入性的活组织检查和非侵入性的成像手段来追踪肿瘤的大小、扩增以及对治疗的响应。这种方法不仅会给患者带来创伤,而且价格昂贵。然而,循环肿瘤细胞(Circulating Tumor Cells,CTCs)检测的出现打破了这一僵局。
CTCs是从肿瘤病灶脱离并播散到血液中的肿瘤细胞,是恶性肿瘤患者出现术后复发和远处转移的重要原因,也是导至肿瘤患者死亡的重要因素。与其他组织学标本如骨髓等相比,外周血标本容易获得,且创伤性小,是临床上常规检测较为理想的标本来源。
近几年CTCs在肿瘤诊断、监控等方面的临床表现逐渐崭露头角,是目前最具发展潜力的肿瘤无创诊断和实时疗效监测手之一。大量实验已经证实CTCs检测有助于肿瘤的早期诊断、判断患者预后、评估抗肿瘤药物的疗效及制定个体化治疗方案。
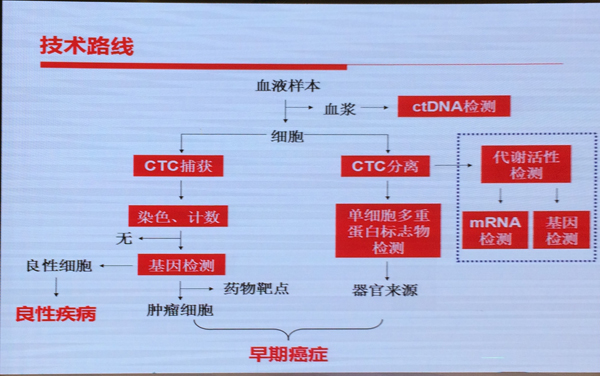
通过CTCs检测进行肿瘤诊断的技术路线
与传统的诊断方法相比,CTCs检测可更加敏感地发现疾病的变化,且对患者没有副作用。不过,想要检测到这些罕见的CTCs非常具有挑战性。因为,在1毫升的患者血液样本中可能只有1-10个这样的细胞,并且它是连续产生的,在血液中呈动态分布,会出现滞后现象,具有很强的异质性。
鉴于CTCs检测表现出的绝对实力和存在的一些障碍,很多来自世界各地的科学家们坚持在该领域奋斗着。近日,在2015年上海市大健康产业发展与合作论坛上,来自上海交通大学生物医学工程学院的青年千人计划专家施奇惠教授以《人外周血中循环肿瘤/上皮细胞的检测》为主题,发表了精彩的演讲。
CTC的技术挑战
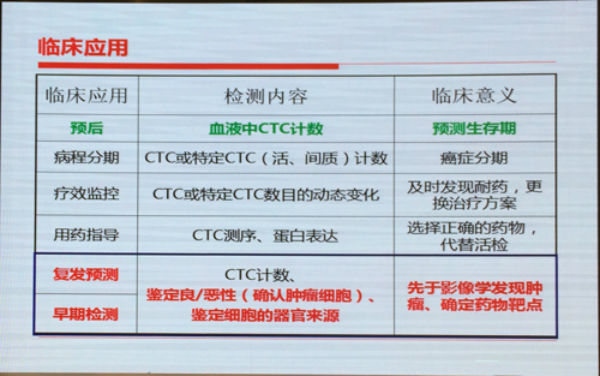
CTCs检测的临床应用
一直以来,血液都是一个很好的检测人体健康的窗口。传统的检测疾病方法是测定分子类标志物,包括蛋白、代谢物、核酸、microRNA、外泌体等。但是,对于癌症检测来说,近十年里,细胞标志物(即从器官组织脱离到血液中的稀有细胞)的检测越来越受关注,其中就包括了CTCs。
如今,CTCs检测已经成为一种新颖的癌症检测手段,但是查找最早的文献可以发现,CTCs的概念早在1869年就由澳大利亚学者Ashworth提出了。然而,经过近150年的发展,该领域却并没有取得很大的进展,原因主要是因为CTCs非常稀有。因此,如何从复杂的血液中鉴定并分离出CTCs是一件非常艰难的工作。
其中,分离的过程需要到达很高的捕获率和纯度,且要保证细胞的活性。此外,由于CTCs数量极少,因此可能会涉及到多种检测整合到单个细胞中。目前,大部分的技术以及临床研究局限于对CTCs的计数,对CTCs分子表征研究的较少。然而,计数的结果可能随着癌细胞脱落速度的改变产生波动,且不同的CTCs的功能异质性大,因此通过CTCs计数得到的信息其实非常有限。
唯一获批的产品:CellSearch系统
目前,美国FDA批准的唯一一种CTC临床检测是杨森诊断公司(Janssen Diagnostics)的CellSearch,它能有效定义上皮来源的CTC。CellSearch是一个半自动化系统,基于EpCAM(上皮细胞抗原)的磁珠捕获、染色,在荧光显微镜下对DAPI+/CK+/CD45-的细胞进行计数。
美国FDA在2004年、2007年和2008年分别批准CellSearch系统用于转移性乳腺癌、结直肠癌与前列腺癌的预后评估、无进展生存期和总生存期的预测。我国CFDA在2012年批准了CellSearch系统用于转移性乳腺癌的预后评估。
其中,2004年发表在NEJM上的题为《Circulating Tumor Cells,Disease Progression, and Survival in Metastatic Breast Cancer》的论文中,研究人员将CellSearch系统用于转移性乳腺癌的预后评估,结果显示,7.5毫升血液中含有5个以下CTC预后较好。
CTC设备大分享,检测原理最强解析
据施教授统计,目前国际上从事CTC设备研发公司有40-50家,下表中列举了部分公司的相关信息。根据检测技术来说,CTC设备主要分为体内检测和体外检测。其中前者是将检测系统留置于体内血管中;目前只有德国的GILUPI公司在开发,属于基于EpCAM抗体的正选。
除此之外,其它的CTC设备都属于体外检测,即通过抽取7.5毫升的血液进行检测。体外检测分为两类,包括不捕获(富集)直接检测和先捕获(富集)后检测,其中后者为主流的检测方法。
先捕获(富集)后检测的方法也分为两类,即正选和负选。正选主要是通过CTC表面标志物或细胞的物理性质(大小、密度)进行捕获;前者是基于免疫磁球技术和微流控芯片技术,后者是基于过滤、离心的原理。负选则是通过白细胞表面标志物间接捕获CTC。

不同捕获方法特征对比
对循环肿瘤细胞良性/恶性的鉴定最可靠的方法是测序,但是成本较贵。另外,病理学鉴定也是一种可选择的方法,但是目前该方法能否对血液中游离的细胞进行可靠的鉴定还没有很多可靠的临床证据。
事实上,血液里除了红细胞、白细胞和CTC以外,还有很多其它类型的细胞,包括成熟的巨核细胞、未成熟的髓细胞以及淋巴样细胞、内皮细胞、鳞状上皮细胞、间皮细胞等。任何分选方法的特异性都是有限的,这些混入的细胞会给后续的检测带来一定的影响。因此,国内外的科学家和相关公司一直在开发新的技术对此进行改进。相信在不久的将来,CTC一定会成在临床肿瘤诊治中得到更广泛的推广应用。
 /3
/3 